
科目: 来源: 题型:阅读理解
| 足量NaOH溶液 |
| 足量稀盐酸 |
| 足量NaOH溶液 |

查看答案和解析>>
科目: 来源: 题型:

| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| ||

查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 实验现象或 预期实验现象 |
现象解释 (用离子方程式表示) |
结论 | |
| 猜想② | 操作一: |
溶液pH=8 | / | Na2S2O3溶液呈中性,能与酸反应,具有还原性,与Na2SO4的化学性质不相似. |
| 操作二: |
S2O32-+2H+=S↓+SO2↑+H2O | |||
| 猜想③ | 操作三: |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ||

查看答案和解析>>
科目: 来源: 题型:
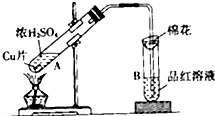 某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.
某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.查看答案和解析>>
科目: 来源: 题型:
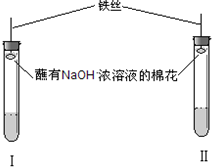
| 实验操作 | 实验现象 | 探究结论 |
| A.取少量品红溶液加入试管Ⅰ中,加入适量碳酸钠溶液,充分混合后再加入一定量的稀硫酸,并立即塞上塞子 | 溶液的红色逐渐褪去,加稀硫酸后溶液逐渐变红色 | CO2 |
| B.取少量品红溶液加入试管Ⅱ中,加入适量亚硫酸钠溶液,充分混合后再加入一定量的稀硫酸,并立即塞上塞子 | 溶液的红色逐渐褪去,加稀硫酸后溶液逐渐变红,随着反应的进行,颜色又逐渐消失 | SO2 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com