
科目: 来源: 题型:
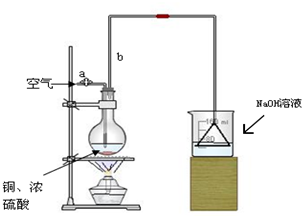 某学校课外活动小组针对教材中铜与浓硫酸反应,提出了“能够与铜反应的硫酸的最低浓度是多少?”的探究课题,并设计了如下方案进行实验:实验试剂:18mol/L硫酸20mL,纯铜粉足量,足量2mol/LNaOH溶液.
某学校课外活动小组针对教材中铜与浓硫酸反应,提出了“能够与铜反应的硫酸的最低浓度是多少?”的探究课题,并设计了如下方案进行实验:实验试剂:18mol/L硫酸20mL,纯铜粉足量,足量2mol/LNaOH溶液.查看答案和解析>>
科目: 来源: 题型:
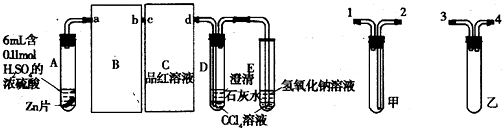
查看答案和解析>>
科目: 来源: 题型:
- 2 |
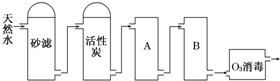
查看答案和解析>>
科目: 来源: 题型:阅读理解
 实验室在没有浓盐酸的情况下,常用浓硫酸、食盐和二氧化锰在加热条件下制取氯气,发生反应的化学方程式为2NaCl+3H2SO4(浓)+MnO2
实验室在没有浓盐酸的情况下,常用浓硫酸、食盐和二氧化锰在加热条件下制取氯气,发生反应的化学方程式为2NaCl+3H2SO4(浓)+MnO2
|
| 选用的仪器 | 加入试剂 |
| A | 食盐粉末、二氧化锰、浓硫酸 |
| B | 紫色石蕊试液 |
| 淀粉-KI溶液 | |
查看答案和解析>>
科目: 来源: 题型:
| A、含中1mol HNO3的浓硝酸和稀硝酸分别与足量铜反应,稀硝酸溶液的铜更多,是因为稀硝酸的氧化能力强于浓硝酸 | B、铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化膜 | C、向AgCl沉淀中逐渐滴加KI溶液,生成黄色沉淀,是因为Ksp(AgCl)<Ksp (AgI) | D、生活中可以使用明矾对饮用水进行消毒、杀菌,是因为明矾能溶于形成胶体 |
查看答案和解析>>
科目: 来源: 题型:
| A、无色试液使红色石蕊试纸变蓝,结论:该试溶一定是碱溶液 | B、无色试液加入盐酸酸化的氯化钡溶液,出现白色沉淀,结论:试液中含有SO42- | C、无色试液焰色反应呈黄色,结论:试液中一定含有Na+ | D、无色试液加入碳酸钠溶液产生白色沉淀,结论:试液中含氢氧化钙 |
查看答案和解析>>
科目: 来源: 题型:
| A、①和③试管内溶液体积不等,溶质物质的量浓度也不相等 | B、因为它们都可溶于水,所以液面都上升到试管顶部 | C、三支试管中,试管②中溶液的溶质的物质的量浓度最小 | D、试管②和试管③中溶液的溶质的物质的量浓度一定相等 |
查看答案和解析>>
科目: 来源: 题型:
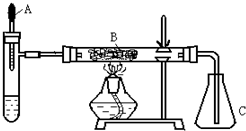 已知多种重金属化合物能催化H2O2的分解.试管中加入过量浓氨水并滴入2ml 5%AgNO3溶液;A为胶头滴管,预先吸有25%的H2O2溶液; B中装有铂石棉催化剂.点燃酒精灯一段时间后,将A中的H2O2溶液慢慢地滴入试管,试管内产生大量气体.不久,锥形瓶C内出现明显的颜色变化.回答下列问题:
已知多种重金属化合物能催化H2O2的分解.试管中加入过量浓氨水并滴入2ml 5%AgNO3溶液;A为胶头滴管,预先吸有25%的H2O2溶液; B中装有铂石棉催化剂.点燃酒精灯一段时间后,将A中的H2O2溶液慢慢地滴入试管,试管内产生大量气体.不久,锥形瓶C内出现明显的颜色变化.回答下列问题:查看答案和解析>>
科目: 来源: 题型:
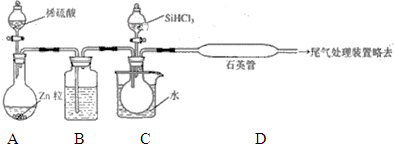
查看答案和解析>>
科目: 来源: 题型:
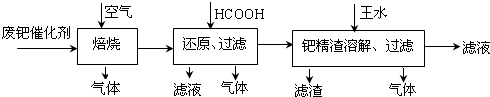
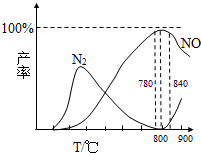
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com