
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 编号 | 改变的条件 | 生成SO3 的速率 |
| ① | 降低温度 | |
| ② | 增大氧气浓度 | |
| ③ | 使用负催化剂 | |
| ④ | 压缩体积 |
| 编号 | 实验操作 | 实验的目的 | ||
| ① | 3毫升5%H2O2 | 1-2滴1mol/LFeCl3 | 5℃左右的冷水的烧杯中 | |
| ② | 3毫升5%H2O2 | 1-2滴1mol/LFeCl3 | 40℃左右的热水的烧杯中 | |
| ③ | 2-3毫升3mol/L的HCl溶液 | 5克CaCO3 | CaCO3固体 | 固体的表面积因素对化学反应速率的影响 |
| ④ | CaCO3粉末 | |||
查看答案和解析>>
科目: 来源: 题型:
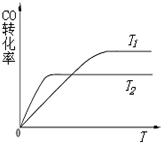 甲醇具有开发和应用广阔的前景.工业上一般采用下列两种途径合成甲醇:
甲醇具有开发和应用广阔的前景.工业上一般采用下列两种途径合成甲醇:| 温度 | 250℃ | 350℃ |
| K | 2.041 | 0.012 |
查看答案和解析>>
科目: 来源: 题型:
| 催化 |
| t/s | 0 | 500 | 1 000 |
| [H2]/mol?L-1 | 5.00 | 3.52 | 2.48 |
| [CO]/mol?L-1 | 2.50 |
查看答案和解析>>
科目: 来源: 题型:
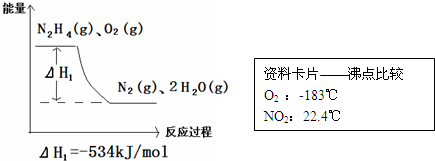
查看答案和解析>>
科目: 来源: 题型:
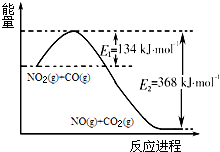 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 温度 | 25℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目: 来源: 题型:
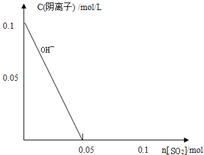
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com