
科目: 来源: 题型:
| ||
查看答案和解析>>
科目: 来源: 题型:
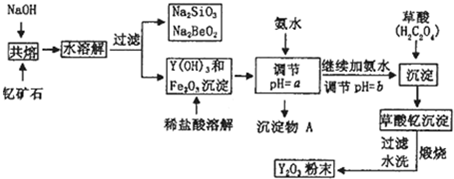
| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | x |
| Y3+ | 6.0 | 8.2 |
查看答案和解析>>
科目: 来源: 题型:
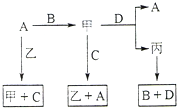 A、B、C、D 是中学化学常见的四种单质,甲、乙、丙为三种化合物,乙在常温下为无色无味的液体,各备物质间转化关系如图:(反应条件已略去),请填空:
A、B、C、D 是中学化学常见的四种单质,甲、乙、丙为三种化合物,乙在常温下为无色无味的液体,各备物质间转化关系如图:(反应条件已略去),请填空:查看答案和解析>>
科目: 来源: 题型:
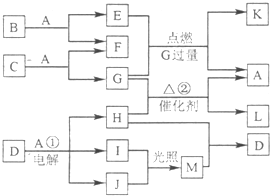 图中的物质均由前20号元素组成,常温下A为液体,E、G、H、I、J、K、L、M为气体,且G、I J为单质;E与M反应的产物是工业上合成某种塑料的单体.
图中的物质均由前20号元素组成,常温下A为液体,E、G、H、I、J、K、L、M为气体,且G、I J为单质;E与M反应的产物是工业上合成某种塑料的单体.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
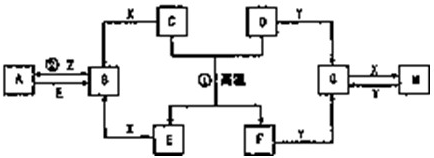
 以下各物质均为中学阶段常见的物质,其中B是单质,它们的转化关系如图所示:
以下各物质均为中学阶段常见的物质,其中B是单质,它们的转化关系如图所示:查看答案和解析>>
科目: 来源: 题型:
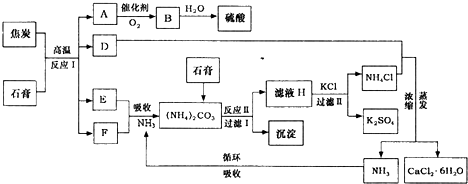
| 压 强/M Pa 转化率/% 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| O | 2- 3 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
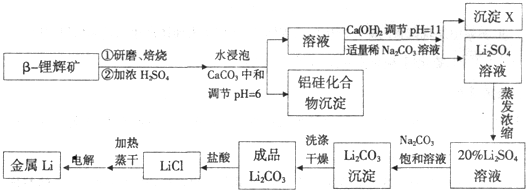
查看答案和解析>>
科目: 来源: 题型:
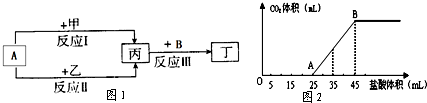
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com