
科目: 来源: 题型:
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是()。
A.反应的化学方程式为:2M N
N
B.t2时,正、逆反应速率相等,反应达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍

查看答案和解析>>
科目: 来源: 题型:
现在工业上主要采用离子交换膜法电解饱和食盐水制取H2、Cl2、NaOH。请回答下列问题:
(1)在电解过程中,与电源正极相连的电极上所发生的电极反应为___________。
(2)电解之前食盐水需要精制,目的是除去粗盐中的Ca2+、Mg2+、 等杂质离子,使用的试剂有:a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,其合理的加入顺序为________(填试剂序号)。
等杂质离子,使用的试剂有:a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,其合理的加入顺序为________(填试剂序号)。
(3)如果在容积为10L的离子交换膜电解槽中,1min在阴极可产生11.2LH2(标准状况下),这时溶液中OH-的物质的量浓度为_______。(设体积维持不变)
(4)Cl2常用于自来水的消毒杀菌,现有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为____________。
查看答案和解析>>
科目: 来源: 题型:
 CO2+2H2O+4Cu,忽略空气中的某些成分对该实验的影响)。
CO2+2H2O+4Cu,忽略空气中的某些成分对该实验的影响)。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
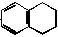 ,分子式为C10H12,常温下为无色液体,有刺激性气味,沸点为207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2
,分子式为C10H12,常温下为无色液体,有刺激性气味,沸点为207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2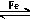 C10H8Br4+4HBr。生成的四溴化萘常温下为固态,不溶于水。有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
C10H8Br4+4HBr。生成的四溴化萘常温下为固态,不溶于水。有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:查看答案和解析>>
科目: 来源: 题型:
 +
+

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
400K、1.01×105Pa时,2L常见烃A的蒸气能在bL氧气中完全燃烧,反应后体积增至(b+4)L(体积在相同的条件下测定)。
(1)烃A在组成上应满足的条件是___________;
(2)当b=15时,该烃可能的化学式为___________;
(3)当A在常压常温下为气态时,b的取值范围是_________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com