
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
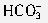 的水称为暂时硬水,加热可除去Ca2+、Mg2+变为软水。现有一锅炉尝试用这种水,试判定其锅垢的主要成分为( )。
的水称为暂时硬水,加热可除去Ca2+、Mg2+变为软水。现有一锅炉尝试用这种水,试判定其锅垢的主要成分为( )。查看答案和解析>>
科目: 来源: 题型:
有甲、乙两份等体积的浓度均为0.1mol?L-1的氨水,pH为11。
(1)甲用蒸馏水稀释100倍,则NH3?H2O的电离平衡将向________(填“促进”或“抑制”)电离的方向移动,溶液的pH将为________(填序号)。
A.9~10之间 B.11 C.12~13之间 D.13
(2)乙用0.1mol?L-1的氯化铵溶液稀释100倍,稀释后的乙溶液与稀释后的甲溶液相比较,pH_____(填“甲大”、“乙大”或“相等”),其原因是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com