
科目: 来源: 题型:
图1和图2分别是1s电子的概率分布图和原子轨道图。下列有关认识正确的是()。

A.图1中的每个小黑点表示1个电子
B.图2表示1s电子只能在球壳内出现
C.图2表明1s轨道呈圆形,有无数对称轴
D.图1中的小黑点表示电子在原子核外出现的概率
查看答案和解析>>
科目: 来源: 题型:
参考下表中数据,回答有关问题: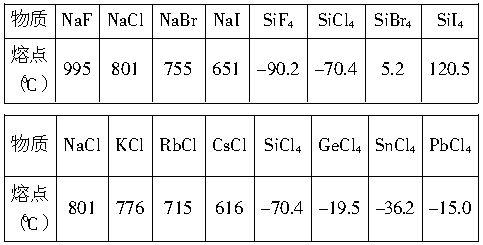
(1)钠的卤化物及碱金属的氯化物的熔点与___________有关,随___________增大,___________减小,故熔点依次降低。
(2)硅的卤化物及硅、锗、锡、铅的氯化物的熔点与_________有关,随着_________增大,___________增强,故熔点依次升高。
(3)钠的卤化物的熔点比相应的硅的卤化物的熔点高得多,这与_________有关,因为___________________________________,故前者熔点远远高于后者。
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
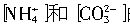 的等式:__________________。
的等式:__________________。查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com