
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 SiHCl3+H2。
SiHCl3+H2。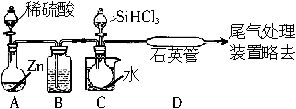
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
已知:Sn(s)+Cl2(g)=SnCl2(s) ΔH1=-349.8kJ?mol-1,SnCl2(s)+Cl2(g)=SnCl4(s) ΔH2=-195.4kJ?mol-1。则在一定条件下,生成SnCl4(s)的热化学方程式为()。
A.Sn+2Cl2=SnCl4 ΔH(298K)=-154.4kJ?mol-1
B.Sn(s)+2Cl2(g)=SnCl4(s) ΔH(298K)=-545.2kJ
C. Sn(s)+2Cl2(g)=SnCl4(s) ΔH(298K)=-154.4kJ?mol-1
D. Sn(s)+2Cl2(g)=SnCl4(s) ΔH(298K)=-545.2kJ?mol-1
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
某化学学习小组的同学们拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量而生成NaHCO3,他们设计了如下实验步骤: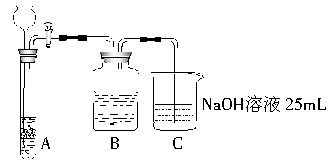
①取25mLNaOH溶液吸收过量的CO2气体,至CO2气体不再溶解(如上图所示,夹持及支撑装置未出)。
②小心煮沸溶液。
③在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。
(1)步骤②的目的是什么?操作时要注意些什么?
(2)他们能否制得较纯净的Na2CO3?___________,理由是_______________________________________。
(3)装置A中盛放的试剂是石灰石和盐酸溶液,可否使用纯碱代替石灰石?
(4)装置B中盛放的试剂是___________________,其作用是_____________________________________。
(5)有同学认为步骤②③对调,即先混合再煮沸,更合理,你认为对吗?为什么?
(6)有同学认为直接向50 mLNaOH溶液中通入足量CO2后,将所得溶液充分加热也可得到纯净的Na2CO3溶液,你认为他能否得到纯净的Na2CO3溶液?如果你认为能得到纯净的Na2CO3溶液,请与学习小组的同学们设计的方案进行比较,看哪种方案更节约药品(如果你认为不能得到纯净的Na2CO3溶液,不必评论)?
(7)如何检验他们得到的溶液是不含NaHCO3的纯净的Na2CO3溶液?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com