
科目: 来源: 题型:
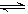 2Z(g)(正反应为放热反应),当反应到达平衡时,升高温度,对反应产生的影响正确的是( )。
2Z(g)(正反应为放热反应),当反应到达平衡时,升高温度,对反应产生的影响正确的是( )。查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按曲线b进行,可采取的措施是( )。
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按曲线b进行,可采取的措施是( )。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
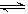 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol?L-1、0.3mol?L-1、0.08mol?L-1,则下列判断不合理的是( )。
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol?L-1、0.3mol?L-1、0.08mol?L-1,则下列判断不合理的是( )。查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com