
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
某学生课外活动小组利用图示装置做如下实验:
在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后又恢复到无色,则此溶液可能是____________溶液,加热时溶液由无色变为红色的原因是______。

查看答案和解析>>
科目: 来源: 题型:
某溶液中含有NO3-、Cl-、AlO2- 、S2-四种离子,若先向其中加入过量的盐酸溶液,微热并搅拌,再加入过量的NaOH溶液,溶液中大量减少的阴离子是()。
A.Cl- B.NO3- C.AlO2- D.S2-
查看答案和解析>>
科目: 来源: 题型:
 MnCl2+Cl2↑+2H2O,设Mn元素全部以Mn2+的形成存在于反应后的溶液中),又收集到bmol单质气体。
MnCl2+Cl2↑+2H2O,设Mn元素全部以Mn2+的形成存在于反应后的溶液中),又收集到bmol单质气体。查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
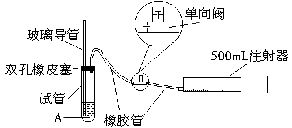
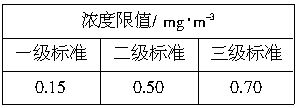
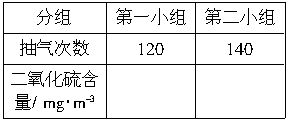
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com