
科目: 来源: 题型:
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
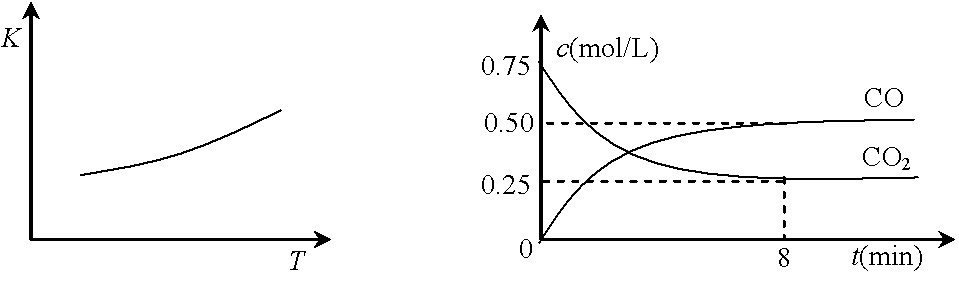
图甲 图乙
⑴该反应的平衡常数表达式K= ▲ 。
⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图乙所示。
8分钟内,CO的平均反应速率v(CO)= ▲ mol/(L·min)。
⑶下列措施中能使平衡时c(CO)/c(CO2)增大的是 ▲ (填序号)。
A.升高温度 B.增大压强
C.充入一定量CO D.再加入一些铁粉
⑷铁的重要化合物高铁酸钠是一种新型饮用水消毒剂,具有氧化能力强、安全性好等优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是 ▲ 。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是 ▲ 。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化纳和水,该反应的离子方程式为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
已知下图中A为单质,D为气体,E和H均为白色沉淀,其中H不溶于稀硝酸,反应中的水和部分产物已略去。
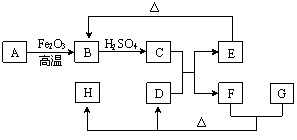
根据框图回答问题:
⑴D的化学式为 ▲ 。
⑵写出“A→B”发生反应的化学方程式 ▲ 。
⑶若在C的溶液中逐滴滴加G溶液,生成的沉淀先增多,后减少,分别写出上述过程中发生反应的离子方程式 ▲ 、 ▲ 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
江苏有着丰富的海水资源,海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。合理利用资源和保护环境是我省可持续发展的重要保证。
⑴海水经过处理后可以得到无水氯化镁,无水氯化镁是工业制取镁的原料。试写出由无水氯化镁制取金属镁的化学反应方程式 ▲ 。
⑵某化工厂生产过程中会产生含有Cu2+和Pb2+的污水。排放前拟用沉淀法除去这两种离子,根据下列数据,你认为投入 ▲ (选填“Na2S”或“NaOH”)效果更好。
难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |
⑶火力发电在江苏的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
①天然海水的pH≈8,试用离子方程式解释天然海水呈弱碱性的原因 ▲ (任写一个)。
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如右图所示。
请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议: ▲ 。
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,使用氧气将其氧化的化学原理是 ▲ (任写一个化学方程式或离子方程式)。氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
)工业上用“三氯氢硅还原法”提纯粗硅的工艺流程如下图所示:
⑴三氯氢硅的制备原理:Si(s)+3HCl(g)![]() SiHCl3(g)+H2(g) △H=-210 kJ/mol
SiHCl3(g)+H2(g) △H=-210 kJ/mol
工业上为了加快SiHCl3生成速率而又不降低硅的转化率,可以采用的方法是 ▲ 。
⑵除上述反应外,还伴随着副反应:Si(s)+4HCl(g)![]() SiCl4(g)+2H2(g) △H=-241 kJ/mol。已知:SiHCl3、SiCl4常温下均为液体。
SiCl4(g)+2H2(g) △H=-241 kJ/mol。已知:SiHCl3、SiCl4常温下均为液体。
①工业上分离SiHCl3、SiCl4的操作方法为 ▲ 。
②反应SiHCl3(g)+HCl(g) ![]() SiCl4(g)+H2(g)的△H= ▲ kJ/mol。
SiCl4(g)+H2(g)的△H= ▲ kJ/mol。
⑶该生产工艺中可以循环使用的物质是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
⑴4FeO·Cr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
⑵2Na2CrO4+H2SO4![]() Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法正确的是
A.反应⑴和⑵均为氧化还原反应
B.反应⑴的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4
D.生成1mol的Na2Cr2O7时共转移7mol电子
查看答案和解析>>
科目: 来源: 题型:
下列各组离子在溶液中一定能大量共存而且呈无色的是
A.Na+、Fe3+、SO42-、NO3- B.OH-、Ba2+、HCO3-、Cl-
C.H+、Mg2+、Cl-、NO3- D.K+、H+、ClO-、S2-
查看答案和解析>>
科目: 来源: 题型:
下列现象或反应的原理解释正确的是
现象或反应 | 原理解释 | |
A. | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔对熔化的铝有较强的吸附作用 |
B. | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
C. | 镀层破损后,镀锡铁比镀锌铁易腐蚀 | 锡比锌活泼 |
D. | 2CO=C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S<0 |
查看答案和解析>>
科目: 来源: 题型:
下列实验操作能够达到目的的是
A.用金属钠除去乙醇中混有的少量水
B.用足量铁粉和氯气直接反应制FeCl2固体
C.用激光笔鉴别Fe(OH)3胶体和Fe(SCN)3溶液
D.用铂丝蘸取某溶液于无色火焰上灼烧,火焰呈黄色,证明其中不含K+
查看答案和解析>>
科目: 来源: 题型:
下列有关金属及其化合物的说法中正确的是
A.钠在空气中燃烧生成淡黄色的Na2O
B.常温下铝制容器可储运浓硫酸或浓硝酸
C.铁在高温下与水蒸气反应生成Fe2O3和H2
D.FeCl2溶液中滴加KSCN溶液时变红色
查看答案和解析>>
科目: 来源: 题型:
下列表示物质结构的化学用语或模型图正确的是
A.HClO的结构式:H-O-Cl B.H2O2的电子式:H+[∶![]() ∶
∶![]() ∶] 2-H+
∶] 2-H+
C.CO2的比例模型:![]() D.14C的原子结构示意图:
D.14C的原子结构示意图:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com