
科目: 来源: 题型:
脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源,
1.硫化氢与氯化铁溶液反应生成单质硫,其离子方程式为_____________________________
2.用过量NaOH溶液吸收硫化氢后,以石墨作电极电解该溶液可回收硫,其电解总反应方程式(忽略氧的氧化还原)为__________________;该方法的优点是____________________.
3.一定温度下,1molNH4HS固体在定容真空容器中可部分分解为硫化氢和氨气,
当反应达到平衡时,P氨气×P硫化氢=a(Pa2)则容器中的总压为________________Pa
题26图是上述反应过程中生成物浓度随时间变化的示意图,若t2时增大氨气的浓度且在t3时反应再次达到平衡,请在图上画出t2时刻后氨气\硫化氢的浓度时间变化曲线
查看答案和解析>>
科目: 来源: 题型:
用过量的H2SO4、NaOH、NH3·H2O 、NaCl等溶液,按题12图所示步骤分开五种离子,则溶液①、②、③、④是( )
A、①NaCl ②NaOH ③NH3·H2O ④H2SO4
B、①H2SO4 ②NaOH ③NH3·H2O ④NaCl
C、①H2SO4 ②NH3·H2O ③NaOH ④NaCl
D、①NaCl ②NH3·H2O ③NaOH ④H2SO4
查看答案和解析>>
科目: 来源: 题型:
氧氟沙星是常用抗菌药,其结构简式如题9图所示,下列对 氧氟沙星叙述错误的是( )
氧氟沙星叙述错误的是( )
A能发生加成、取代反应
B、能发生还原、酯化反应
c、分子内共有19个氢原子
D 分子内共平面的碳原子多于6
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是( )
A.相同条件下,N2和O3的混合气体与等体积的N2所含的原子数相等
B.等物质的量的甲基(-CH3 )与羟基(-OH)所含的电子数相等
C.常温常压下,28gCO与22.4LO2所含分子数相等
D.16g CH4 18g NH4+所含质子数相等
查看答案和解析>>
科目: 来源: 题型:
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,![]() 减小
减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaCl,一定有c(Na+)= c(Cl-)+ c(ClO-)
D.加入少量水,水的电或平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
下列关于元素的叙述正确的是
A.金属元素与非金属元素能形成共价化合物
B.只有在原子中,质子数才与核外电子数相等
C.目前使用的元素周期表中,最长的周期含有36种元素
D.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.![]() 和
和![]() 互为同位素,性质相似
互为同位素,性质相似
B.常温下,pH=1的水溶液中Na+、NO3-、HCO3-、Fe3+可以大量共存
C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同
D.C(石墨,s)=C(金刚石,s) △H>0,所以石墨比金刚石稳定
查看答案和解析>>
科目: 来源: 题型:
物质的量浓度相同时,下列既能跟NaOH溶液反应、又能跟盐酸溶液中pH最大的是
A.Na2CO3溶液 B.NH4HCO3溶液
C.NaHCO3溶液 D.NaHSO4?溶液
查看答案和解析>>
科目: 来源: 题型:阅读理解
某化学兴趣小组查阅资料得知镁可在氮气中燃烧生成Mg3N2,并设计如下实验方案进行探究。
步骤1:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、胶塞等装配如图所示的装置。另准备一只胶塞,其中有一根铜丝穿过,铜丝末端固定一根镁条备用。
步骤2:引燃燃烧匙中的试剂,塞好瓶塞。燃烧结束后,调节广口瓶内外液面相平。
步骤3:点燃镁条,更换胶塞,镁条继续燃烧,反应结束后,广口瓶内水面上升。
步骤4:取蒸发皿中得到的固体,加盐酸溶解。向溶液中加入过量氢氧化钠溶液,有白色沉淀生成,同时得到一种能使湿润红色石蕊试纸变蓝的气体。
⑴为除去广口瓶中的氧气,燃烧匙中应装入下列试剂中的 ▲ (填序号)。
A.炭粉 B.硫粉 C.红磷
⑵“步骤2”中调节内外液面相平的方法: ▲ 。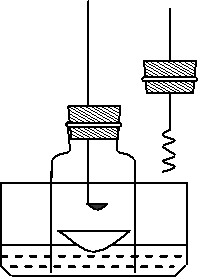
⑶写出Mg3N2溶于足量盐酸生成两种氯化物的化学方程式: ▲ 。
⑷某同学直接将镁条在空气中点燃,并将所得白色固体进行“步骤4”的实验,结果无气体生成,其原因是 ▲ 。
⑸兴趣小组同学为比较镁和铝的金属性强弱,设计了下表中的实验方案一,请你再设计一种不同的实验方案。
实验试剂和用品:镁条、铝条、0.1mol/L MgCl2溶液、0.1mol/L AlCl3溶液、0.1mol/L HCl溶液、 0.1mol/L NaOH溶液、pH试纸(其他实验仪器可任选)
实验操作 | 实验现象 | |
方案一 | 取已除去表面氧化膜的镁条和铝条,分别和0.1mol/L HCl溶液反应 | 均有气泡产生,镁条反应比铝条反应更剧烈 |
方案二 | ▲ | ▲ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com