
科目: 来源: 题型:
(10分)A、B、C、D四种元素的原子序数均小于18,其最高正价数依次为1,4,5,7,已知B的原子核外次外层电子数为2。A、C原子的核外次外层电子数为8。D元素的最高价氧化物对应的水化物是已知含氧酸中最强酸,则:
(1)A的离子结构示意图是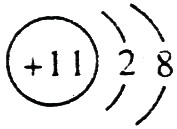 ,C的原子结构示意图是
,C的原子结构示意图是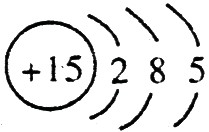 。
。
(2)C的最高价氧化物对应的水化物与A的氢氧化物生成三种盐,化学式分别为Na3PO4、Na2HPO4、NaH2PO4。
(3)C、D的气态氢化物稳定性由强到弱的顺序是 HCl>PH3。
【解析】 最高正价=原子最外层电子数,B元素的原子最外层电子数应为4,B元素原子的次外层电子数为2,为K层,B元素原子核外共有2+4=6个电子,B是6号元素碳;A、C原子次外层电子数为8,则A、C原子核外电子数分别是:2+8+1=11和2+8+5=15,所以A为11号元素钠,C为15号元素磷;在1~18号元素中,最高价为+7的只有氯元素(F无正价),而HClO4是已知含氧酸中最强的酸,故D为氯。
(1)钠总是+1价,其离子结构示意图为: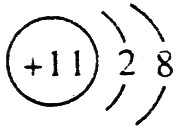 ;磷的原子序数是15,其原子结构示意图是:
;磷的原子序数是15,其原子结构示意图是: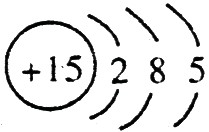 。
。
(2)磷的最高价(+5)氧化物对应的水化物是H3PO4,与NaOH反应生成:Na3PO4、NaH2PO4三种盐。
(3)P、Cl原子都具有3个电子层,核电荷数P(15)小于Cl(17),原子半径r(P)>r(Cl),所以非金属Cl>P,气态氢化物稳定性HCl>PH3。
查看答案和解析>>
科目: 来源: 题型:
(10分)A、B、C、D分别是由两种短周期元素组成的常见微粒(或粒子),这四种微粒中均含有相同数目的电子,且共含有三种元素。其中A中含有5个原子核,它们之间有如下的反应关系:

(1)A、D的电子式分别为:A  ,D
,D 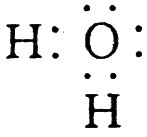 。
。
(2)B、C、D三种微粒结合质子能力x>y>z,(x、y、z分别代表B、C、D中的某一种微粒),则x、y、z分别代表的微粒符号为x OH- ,y NH3 ,z H2O 。
【解析】 A中含5个原子核,又由C+H+→A,推知A为NH![]() ,知C为NH3,B为OH-,D为H2O。
,知C为NH3,B为OH-,D为H2O。
查看答案和解析>>
科目: 来源: 题型:
(8分)A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象:
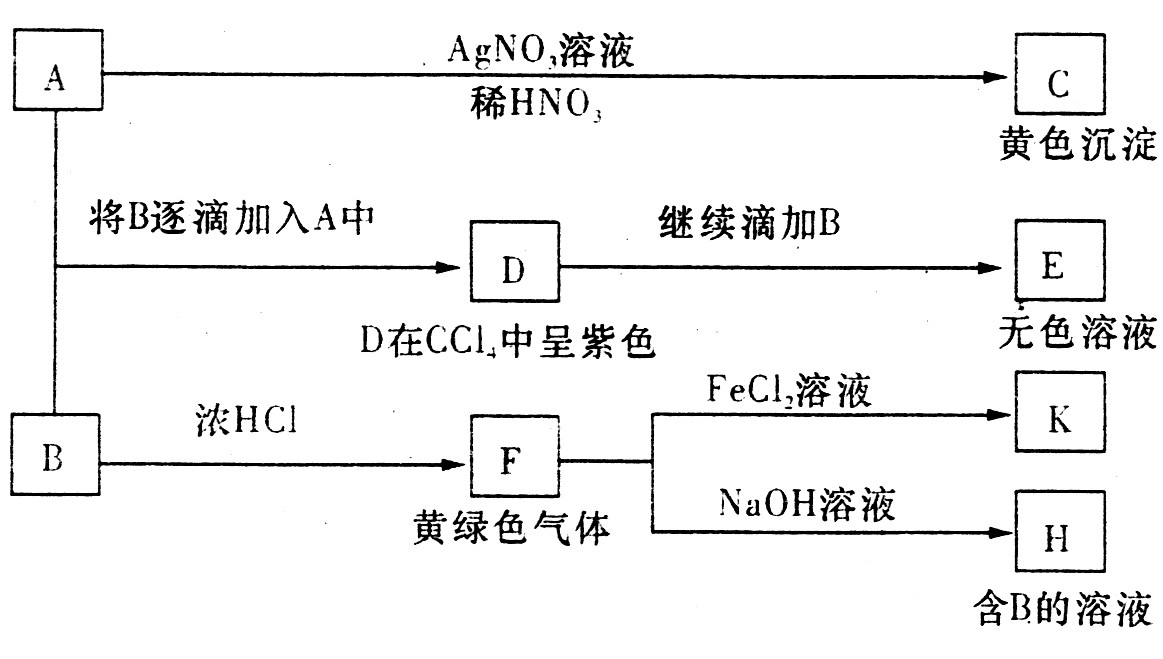
请回答:
(1)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
(2)写出将SO2气体通入K溶液中发生反应的离子方程式:
(3)写出由F→H的化学方程式:
查看答案和解析>>
科目: 来源: 题型:
已知2KCl(固体)+H2SO4(浓)![]() K2SO4+2HCl↑,则实验室用该原理制取HCl的发生装置与实验室制 氯气 (填气体名称)相同,将制和HCl气体溶于水即得盐酸,吸收时用倒置的漏斗。现用实验室 O2(以KClO3为原料,MnO2作催化剂)的残渣为原料,先制得HCl,再制取Cl2。
K2SO4+2HCl↑,则实验室用该原理制取HCl的发生装置与实验室制 氯气 (填气体名称)相同,将制和HCl气体溶于水即得盐酸,吸收时用倒置的漏斗。现用实验室 O2(以KClO3为原料,MnO2作催化剂)的残渣为原料,先制得HCl,再制取Cl2。
(1)某学生提出的实验步骤依次是:溶解、蒸发、结晶、制气体。其中还缺少的必要步骤是 ;
(2)某学生开列的实验用品为:烧杯、圆底烧瓶、蒸发皿、量筒、集气瓶、分液漏斗、酒精灯、药匙、托盘天平、铁架台(含铁夹、铁圈)、双孔橡皮塞、玻璃导管、橡皮管、火柴、蒸馏水。所缺少的必要试剂是 ,还缺少的必要的实验用品是 。
(3)写出制得的HCl溶液与MnO2反应制Cl2的离子方程式: 。
(4)甲同学用51.33 g的MnO2和足量浓盐酸共热制取Cl2的质量为m g。乙同学用200 mL 36.5%的浓盐酸(ρ=1.18 g/cm3)和足量的MnO2共热制取Cl2,得到Cl2的质量为n g。砂考虑反应物的损耗的前提下,m与n的大小关系是m n(填>、<、=)。
(5)多余的Cl2吸收的装置中所用的仪器是 ,试剂是 (选填序号:A. NaOH饱和溶液,B. Ca(OH)2饱和溶液),你选择的理由是 。
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C、D的原子序数都不超过18,它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则下列叙述正确的是( )
A. 原子序数:a>b>c>d
B. 离子半径:A(n+1)+>Bn+>C(n+1)->Dn-
C. 离子还原性:A(n+1)+>Bn+,离子氧化性:C(n+1)->Dn-
D. 单质还原性:B>A,单质氧化性:D>C
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z在周期表中的位置关系如图所示,下列有关叙述正确的是( )
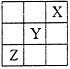
A. Z与铁反应生成的化合物中铁元素显正三价
B. X的最高价氧化物的水化物是一种强酸
C. 1 mol单质Y跟足量水反应时,转移1 mol电子
D. Z有ZO2、ZO3两种氧化物
查看答案和解析>>
科目: 来源: 题型:
同温同压同体积的两个密闭容器中分别充满12C18O和14N2两种气体。关于这两个容器中气体的说法正确的是( A )
A. 质子数相等,质量不等 B. 分子数和质量都不相等
C. 分子数和质量都相等 D. 原子数和中子数都相等
【解析】 根据阿伏加德罗定律,同温同压同体积的12C18O和14N2具有相同的分子数,而12C18O和14N2每个分子中都含14个质子,故质子数也相等,但因为二者的相对分子质量不同,故质量不同。
查看答案和解析>>
科目: 来源: 题型:
氰(CN)2、硫氰(SCN)2等称为拟卤素,它们与卤素单质性质相似,它们的阴离子也与卤素阴离子性质相似。例如:
2Fe+3(SCN)2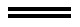 2Fe(SCN)3
2Fe(SCN)3
Ag++CN-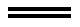 AgCN↓(白)
AgCN↓(白)
拟卤素形成的无氧酸和含氧酸一般比氢卤酸和次卤酸弱。下列反应中,不正确的是( C )
A. 2CN-+Cl2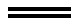 2Cl-+(CN)2
2Cl-+(CN)2
B. (CN)2+2OH-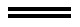 CN-+CNO-+H2O
CN-+CNO-+H2O
C. (CN)2+H2O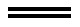 2H++CN-+CNO-
2H++CN-+CNO-
B. MnO2+4HSCN (SCN)2+Mn(SCN)2+2H2O
(SCN)2+Mn(SCN)2+2H2O
【解析】 从题中信息可以看出,拟卤素形成的无氧酸和含氧酸均为弱酸,书写离子方程式时不能拆开成离子。
查看答案和解析>>
科目: 来源: 题型:
同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3 ②NO2,进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度为( )
A. ①>② B. ①<② C. ①=② D. 不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com