
科目: 来源: 题型:
某温度下在密闭容器中发生如下反应:![]() =2E(g),若开始时只充入2mol E(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2mol M和1mol N 的混合气体达平衡时M的转化率 ( )
=2E(g),若开始时只充入2mol E(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2mol M和1mol N 的混合气体达平衡时M的转化率 ( )
A.20% B.40% C.60% D.80%
查看答案和解析>>
科目: 来源: 题型:
反应2SO2+O2 2SO2经一段时间后,SO3的浓度增加了0.4mol?L-1,在这段时间内用O2表示的反应速率为0.04mol?L-1?s-1,则这段时间为 ( )
A.0.1s B.2.5s C.5s D.10s
查看答案和解析>>
科目: 来源: 题型:
有一种白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验。
(1)逐滴加入6mol?L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液
(2)加热试管中的白色粉末,试管口有水滴凝结
(3)逐滴加入6mol?L-1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管口还有白色溶物
下列混合物中符合以上实验现象的是 ( )
A.NaHCO3、AgNO3 B.BaCl2、MgCO3
C.NH4HCO3、MgCl2 D.CaCl2?6H2O、Na2CO3
查看答案和解析>>
科目: 来源: 题型:
抗击“非典”期间,过氧乙酸(CH3C-O-OH)是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
① □MnO4+□H2O2+□H+ == □Mn2++□O2十□H2O
② H2O2+2![]() +2H+ === I2+2H2O
+2H+ === I2+2H2O
③ CH3C-O-OH+2![]() +2H+ === CH3COOH+I2+H2O
+2H+ === CH3COOH+I2+H2O
请回答以下问题:
(l)配平反应①的离子方程式(配平系数填人以下方框内):
□MnO4+□H2O2+□H+ === □Mn2++□O2十□H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是____________________。
(3)取b0 mL待测液,用硫酸使溶液酸化,再用浓度为a1 mol?![]() 的KmnO4标准溶液
的KmnO4标准溶液
滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中KmnO4不与过氧乙酸反应)。
另取b0 mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2 mol?![]() 的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。
c0= ________________________。
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果 _______________(填是或否)
查看答案和解析>>
科目: 来源: 题型:
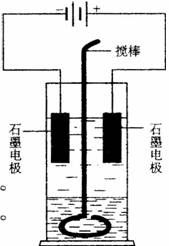
在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
(1)阳极上的电极反应式为_____________________。
(2)阴极上的电极反应式为_____________________。
(3)原上层液体是_____________________________。
(4)原下层液体是______________________________。
(5)搅拌后两层液体颜色发生变化的原因是________
。
(6)要检验上层液体中含有的金属离子,其方法是_____________________________,
现象是_______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
请回答下列问题:
(1)已知M的分子量为227,由C、H、O、N周四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是_____________________。D是双原子分子,分子量为30,则D的分子式为________________。
(2)油脂A经下列途径可得到M。
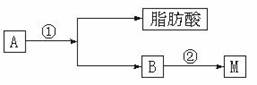
图中②的提示:
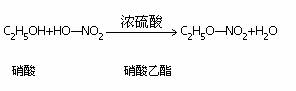
反应①的化学方程式是
_________________________________________________________________________。
反应②的化学方程式是
_________________________________________________________________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,分子量为134,写出C所有可能的结构简式
_________________________________________________________________________。
(4)若将0.1mol B与足量的金属钠反应,则需消耗_________g金属钠。
查看答案和解析>>
科目: 来源: 题型:
粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.15 L 6.0 mol?![]() 盐酸中,得溶液C;
盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出 l.12 L(标况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是_______________________________________,产物中的单质B是__________________。
(2)②中所发生的各反应的化学方程式是________________________________________。
(3)③中所发生的各反应的离子方程式是______________________________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为___________________,c(Fe2+)为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com