
科目: 来源: 题型:
已知X、Y、Z都是短周期的元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层电子数的三倍,Y和Z可以形成两种以上的气态化合物,则
(1) Y是 、Z是 (填元素名称)。
(2)由Y和Z组成,且Y和Z质量比为7∶20的化合物的化学式(分子式)是 。
(3)由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种离子是(离子符号) 和 。
(4) X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子的个数比为4∶2∶3,该盐的化学式(分子式)是 。
查看答案和解析>>
科目: 来源: 题型:
某研究小组进行与NH3有关的系列实验。
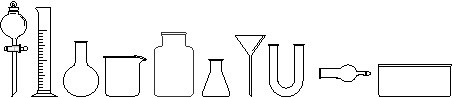
(1)从下图中挑选所需仪器,画出制取干燥NH3的装置简图(添加必要的塞子、玻璃导管、
胶皮管。固定装置和尾气处理装置不用画),并标明所用试剂。
 |
(2)将NH3通入溴水中,有N2生成,反应的化学方程式为 。
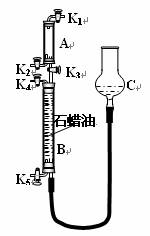
(3)为验证“同温同压下,相同体积的任何气体都含有相同数目的分子”,该小组同学设计了如右上图所示的装置,图中B管的容积是A管的2倍,活塞K1、K2、K3、K4、K5均关闭(固定装置和尾气处理装置略);HCl和NH3均不溶于石蜡油,也不与之反应;装置气密性好。
①在A管中充满与大气压强相等的干燥HCl气体。操作是 。控制活塞K4、K5,调节C,使B管充满与A管同压的干燥NH3。
②缓缓开启K3,A管中的现象是 。要达到实验目的,当反应完成并恢复到室温时,B管中预期的现象是 ;
若观察不到预期现象,主要原因是 。
查看答案和解析>>
科目: 来源: 题型:
晶体硅是一种重要的非金属材料。制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅。
![]() ②粗硅与干燥HCl气体反应制得SiHCl3: Si + 3HCl SiHCl3 + H2
②粗硅与干燥HCl气体反应制得SiHCl3: Si + 3HCl SiHCl3 + H2
③ SiHCl3与过量H2在1000~1100℃反应制得纯硅。
已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为 。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量
SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为:
。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
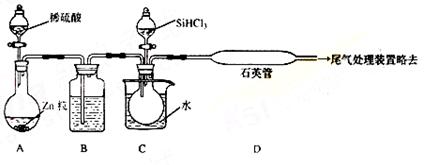
①装置B中的试剂是 ,装置C中的烧瓶需要加热,
其目的是: 。
②装置D不能采用普通玻璃管的原因是 ,
装置D中发生反应的化学方程式为 。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及 。
查看答案和解析>>
科目: 来源: 题型:
某温度下,体积一定的密闭容器中进行如下可逆反应: ( )
X(g) + Y(g) ![]() Z(g) + W(s) △H>0下列叙述正确的是
Z(g) + W(s) △H>0下列叙述正确的是
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应到达平衡
C.升高温度,平衡逆向移动
D.平衡后加入X,上述反应的△H增大
查看答案和解析>>
科目: 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N2(g) + 3H2(g) ![]() 2NH3(g) ,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如
2NH3(g) ,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如
下图所示。下列叙述正确的是 ( )
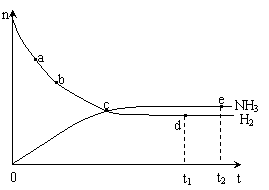 |
A.点a的正反应速率比点b的大
B.点 c处反应达到平衡
C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大
查看答案和解析>>
科目: 来源: 题型:
下列实验中,溶液颜色有明显变化的是 ( )
A.少量明矾溶液加入到过量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固体加入到过量NaHSO3溶液中
D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
查看答案和解析>>
科目: 来源: 题型:
SO42-和 S2O82-结构中,硫原子均位于由氧原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。下列说法正确的是 ( )
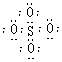 A. SO42-的电子式为
A. SO42-的电子式为
B.S2O82-中没有非极性键
C.S2O82-比SO42- 稳定
D.S2O82-有强氧化性
查看答案和解析>>
科目: 来源: 题型:
某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:Li + LiMn2O4 == Li2Mn2O4 。下列说法正确的是 ( )
A.放电时,LiMn2O4发生氧化反应
B.放电时,正极反应为:Li+ + LiMn2O4 + e- == Li2Mn2O4
C.充电时,LiMn2O4发生氧化反应
D.充电时,阳极反应为:Li+ + e- == Li
查看答案和解析>>
科目: 来源: 题型:
室温时,将x mL pH = a 的稀NaOH溶液与y mL pH = b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是 ( )
A.若x = y,且a + b = 14,则pH > 7
B.若10x = y,且a + b = 15,则pH = 7
C.若ax = by,且a + b = 13,则pH = 7
D.若x = 10y,且a + b = 14,则pH > 7
查看答案和解析>>
科目: 来源: 题型:
下列关于电解质溶液的叙述正确的是 ( )
A.常温下,pH = 7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为
c(Cl-) > c(NH4+) > c(H+) > c(OH-)
B.将pH = 4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com