
科目: 来源: 题型:
2005年10月12日我国成功发射了第二艘载人航天飞船――“神州六号”,实现了双人多天太空旅行。这标志着中国人的太空时代又前进了一大步。发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
已知:N2(g) + 2O2(g) = 2NO2(g); △H = + 67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g); △H = 534kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是( )
A、2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(l);△H = 1135.7kJ/mol
B、2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = 1000.3kJ/mol
C、N2H4(g) + NO2(g) = 3/2N2(g) + 2H2O(l);△H = 1135.7kJ/mol
D、2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = 1135.7kJ/mol
查看答案和解析>>
科目: 来源: 题型:
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:
H2O2 → H2O IO3- → I2 MnO4- → Mn2+ HNO3 → NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A. H2O2 B. IO3- C. MnO4- D. HNO3
查看答案和解析>>
科目: 来源: 题型:
下列有关物质的结构或性质的叙述错误的是( )
A. 由极性键形成的分子不一定是极性分子
B. 水是一种非常稳定的化合物,这是由于氢键所致
C. 石英、食盐、金属钠、干冰的熔点依次降低
D. 分子晶体中一定存在分子间作用力,可能有共价键
查看答案和解析>>
科目: 来源: 题型:
据最新报道,科学家发现了如下反应:O2+PtF6=O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列说法正确的是( )
A.在此反应中,O2是氧化剂,PtF6是还原剂
B.O2(PtF6)中氧元素的化合价是+1价
C.O2(PtF6)中不存在共价键
D.在此反应中,每生成1mol O2(PtF6)则转移1mol电子
查看答案和解析>>
科目: 来源: 题型:
不具有放射性的同位素称之为稳定同位素,近20年来,稳定同位素分析法在植物生理学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用做环境分析指示物。下列说法中正确的是( )
A.34S原子核内的中子数为16
B.1H216O在相同条件下比1H218O更易蒸发
C.13C和15N原子核内的质子数相差2
D.2H+的酸性比1H+的酸性更强
查看答案和解析>>
科目: 来源: 题型:
钴(Co)化合物对化学键的研究起着重要的作用。为测定某钴化合物[ Co(NH3)xCly ]Clz的组成,进行如下实验:
①称取样品0.5010 g,加入过量的NaOH溶液,煮沸,蒸出所有的氨,冷却,得到A。
产生的氨用50.00 mL 0.5000 mol•L-1的盐酸完全吸收并用蒸馏水定容至100 mL,得溶液B。取B溶液20.00 mL, 用0.1000 mol•L-1 NaOH滴定,消耗NaOH溶液30.00 mL。
②向A中加入过量KI固体,振荡,盐酸酸化后置于暗处,发生反应:
Com+ + I- → Co2+ + I2 (未配平)
反应完成后,蒸馏水稀释,用Na2S2O3溶液滴定析出的I2,消耗0.1000 mol•L-1Na2S2O3溶液20.00 mL。反应方程式为:I2 + 2Na2S2O3 == 2NaI + Na2S4O6
③另称取该物质样品0.2505 g溶于水,以0.1000 mol•L-1 AgNO3溶液滴定至恰好反应完全,消耗AgNO3溶液20.00 mL。相应反应式为:
[ Co(NH3)xCly ]Clz + zAgNO3 == [ Co(NH3)xCly ](NO3)z + zAgCl↓
通过计算求:
(1) [ Co(NH3)xCly ]Clz中氮元素的质量分数。
(2)该钴化合物的化学式。
查看答案和解析>>
科目: 来源: 题型:
合成氨工业生产中所用的αFe催化剂的主要成分是FeO、Fe2O3 。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4∶5,其中Fe2+与Fe3+物质的量之比为 。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为 (用小数表示,保留2位小数)。
![]() (3)以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:
2Fe2O3 + C 4FeO + CO2↑。为制得这种活性最高的催化剂,应向480g Fe2O3粉末中
加入炭粉的质量为 g 。
查看答案和解析>>
科目: 来源: 题型:
水体中重金属铅的污染问题备受关注。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、
Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如图所示:
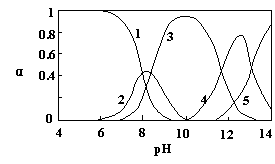 |
【1表示Pb2+,2表示Pb(OH)+,3表示Pb(OH)2、,4表示Pb(OH)3-,5表示Pb(OH)42-】
(1) Pb(NO3)2溶液中,![]() 2(填“>”、“=”、“<”);往该溶液中滴入氯化铵溶液后,
2(填“>”、“=”、“<”);往该溶液中滴入氯化铵溶液后,![]() 增大,可能的原因是 。
增大,可能的原因是 。
(2)往Pb(NO3)2溶液中滴稀NaOH溶液,pH = 8时溶液中存在的阳离子(Na+除外)有
,pH = 9时,主要反应的离子方程式为 。
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- | ||
| 处理前浓度/(mg?L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 | ||
| 处理后浓度/(mg?L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
上表中除Pb2+外,该脱铅剂对其它离子的去除效果最好的是 。
(4)如果该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:
2EH(s) + Pb2+![]() E2Pb(s) + 2H+
E2Pb(s) + 2H+
则脱铅的最合适pH范围为 (填代号)。
A.4~5 B.6~7 C.9~10 D.11~12
查看答案和解析>>
科目: 来源: 题型:
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示 ,
K值大小与温度的关系是:温度升高,K值 。
(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g) + H2O(g) ![]() CO2(g) + H2 (g) △H1 <0
CO2(g) + H2 (g) △H1 <0
CO和H2O浓度变化如下图,则 0~4min的平均反应速率v(CO)= mol/(L•min)
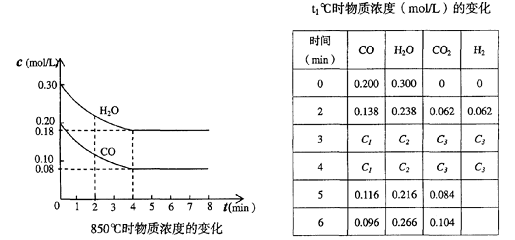
(3) t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于 状态;
C1数值 0.08 mol/L (填大于、小于或等于)。
②反应在4min~5min之间,平衡向逆方向移动,可能的原因是 (单选),
表中5min~6min之间数值发生变化,可能的原因是 (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目: 来源: 题型:
往有机聚合物中添加阻燃剂,可增加聚合物的使用安全性,扩大其应用范围。例如,在某聚乙烯树脂中加入等质量由特殊工艺制备的阻燃型Mg(OH)2,树脂可燃性大大降低。该Mg(OH)2的生产工艺如下:
![]()
(1)精制卤水中的MgCl2与适量石灰乳反应合成碱式氯化镁[Mg(OH)2-xClx•mH2O],
反应的化学方程式为 。
(2)合成反应后,继续在393K~523K下水热处理8h,发生反应:
[Mg(OH)2-xClx•mH2O]== (1-![]() ) Mg(OH)2 +
) Mg(OH)2 +![]() MgCl2 + mH2O
MgCl2 + mH2O
水热处理后,过滤、水洗。水洗的目的是 。
(3)阻燃型Mg(OH)2具有晶粒大,易分散、与高分子材料相容性好等特点。上述工艺流
程中与此有关的步骤是 。
(4)已知热化学方程式:
Mg(OH)2(s) == MgO(s) + H2O(g) △H1 = +81.5 kJ?mol-1
Al(OH)3(s) == ![]() Al2O3(s) +
Al2O3(s) + ![]() H2O(g) △H 2 = +87.7 kJ?mol-1
H2O(g) △H 2 = +87.7 kJ?mol-1
①Mg(OH)2和Al(OH)3起阻燃作用的主要原因是 。
②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是 ,
原因是 。
(5)常用阻燃剂主要有三类:A.卤系,如四溴乙烷;B.磷系,如磷酸三苯酯;C.无机类,
主要是Mg(OH)2和Al(OH)3。从环保的角度考虑,应用时较理想的阻燃剂是
(填代号),理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com