
科目: 来源: 题型:
Marnellos和Stoukides发明了电化学制备氨气方法,该方法用SCY陶瓷将阳极和阴极隔开,SCY陶瓷具有高质子导电性,其作用是传递H+,这种方法实现了高温常压下高转化率的电化学合成氨。已知阳极发生的电极反应为:H2-2e![]() =2H+,则阴极的电极反应式为 。
=2H+,则阴极的电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
如果一个反应的△H-T△S<0,则该反应能够自发进行。已知该反应的△S= -198.2J?K![]() ?mol
?mol![]() 。请判断上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
。请判断上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
查看答案和解析>>
科目: 来源: 题型:
由氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2(g)+3H2(g)![]() 2NH3(g)。已知,在常温下,1g H2完全转化为NH3,放出的热量为15.4 kJ。①请写出该反应的热化学方程式 。常温下,将10mol N2和30mol H2放入合成塔中,充分反应,则放出的热量 (填“等于”、“大于”或“小于”)924 kJ。
2NH3(g)。已知,在常温下,1g H2完全转化为NH3,放出的热量为15.4 kJ。①请写出该反应的热化学方程式 。常温下,将10mol N2和30mol H2放入合成塔中,充分反应,则放出的热量 (填“等于”、“大于”或“小于”)924 kJ。
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组利用细废铁屑制取FeCl3?6H2O晶体。主要步骤如下:
①洗净后的废铁屑放在烧杯内,用过量的工业盐酸浸泡至不再产生气泡,过滤;
②按下图组装仪器,并检查装置的气密性,然后将①得到的滤液放入试剂瓶B中;
③将石墨电极X、Y连接上直流电源,通电,待FeCl2全部被氧化后,断开电源;
④试剂瓶B中的溶液经过一系列实验操作,可得到FeCl3?6H2O晶体。
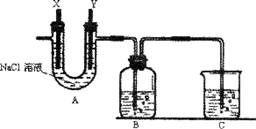
请回答下列问题:
(1)A中的X极应连接电源的 极,
A中发生反应的化学方程式是 ;
B中溶液颜色的变化是 ;
B中反应的离子方程式是 。
(2)烧杯C中应盛放的试剂是 ,
其作用是 。
(3)试剂瓶B中的溶液由步骤④制得FeCl3?6H2O晶体,步骤④需要进行的实验操作依次是(填序号)
A.蒸发浓缩 B.洗涤 C.过滤 D.冷却结晶
(4)在整个实验过程中,盐酸必须保持过量,主要原因是
。
查看答案和解析>>
科目: 来源: 题型:
mA(s)+nB(g)![]() qC(g)△H<0的可逆反应,在一定温度下的密闭容器中进行,平衡时B的体积分数V(B)%与压强(P)关系如下图所示,下列叙述正确的是( )
qC(g)△H<0的可逆反应,在一定温度下的密闭容器中进行,平衡时B的体积分数V(B)%与压强(P)关系如下图所示,下列叙述正确的是( )
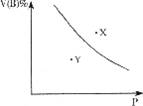
A.n>q B.X点时的状态,V(正)<V(逆)
C.m+n<q D.X点比Y点混和物的正反应速率慢
查看答案和解析>>
科目: 来源: 题型:
已知热化学反应方程式:
![]()
![]()
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)==ZnO(s)+Hg(1)的△H为( )
A.△H=+260.7kJ?mol![]() B.△H= ―260.7kJ?mol
B.△H= ―260.7kJ?mol![]()
C.△H= 一442.3kJ?mol![]() D.△H=+442.3kJ?mol
D.△H=+442.3kJ?mol![]()
查看答案和解析>>
科目: 来源: 题型:
常温时,将HA和HB两种一元酸溶液分别加水稀释,其pH变化如下图所示。下列叙述中正确的是( )
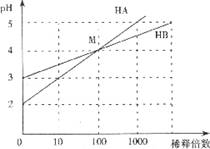
A.HA、HB都是弱酸 B.在M点,c(![]() )=c(
)=c(![]() )
)
C.稀释前,c(HA)=10c(HB) D.在M点,HA、HB酸的电离常数相同
查看答案和解析>>
科目: 来源: 题型:
工业上将苯的蒸气通过赤热的铁能合成一种可作传热载体的化合物。该化合物分子中苯环上的一氯代物有3种。1mol该化合物催化加氢时最多消耗6molH2。这种化合物可能是( )
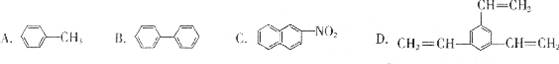
查看答案和解析>>
科目: 来源: 题型:
下列有关沉淀溶解平衡的说法正确的是( )
A.KSP(AB2)小于KSP(CD),则AB2的溶解度小于CD的溶解度
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大
C.在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动
查看答案和解析>>
科目: 来源: 题型:
近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2==2CO2+3H2O,下列说法不正确的是( )
A.乙醇在电池的负极上参加反应
B.1mol CH3CH2OH被氧化转移6mol电子
C.在外电路中电子由负极沿导线流向正极
D.电池正极的电极反应为4H++O2+4e-==2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com