
科目: 来源: 题型:
在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:
H2(g) + I2(g)![]() 2HI(g)
2HI(g) ![]() H<0反应中各物质的浓度随时间变化情况如图1:
H<0反应中各物质的浓度随时间变化情况如图1:

(1)该反应的化学平衡常数表达式为 。
(2)根据图1数据,反应开始至达到平衡时,平均速率v(HI)为 。
(3)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K (填写增大、减小或不变)
HI浓度的变化正确的是 (用图2中a-c的编号回答)
②若加入I2,H2浓度的变化正确的是 ,(用图2中d-f的编号回答)
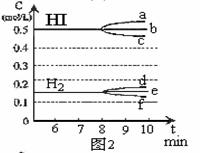
(4)反应达到平衡后,第8分钟时,若反容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况。

查看答案和解析>>
科目: 来源: 题型:
工业上制取CuCl2的生产流程如下:

请结合下表数据,回答下列问题:
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 溶度积/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
(1) 向含有等浓度Fe2+、Cu2+、Fe3+的混合溶液中滴加NaOH溶液,最先生成的沉淀是 。
(2) 溶液A中加入NaClO的目的是 。
(3) 在溶液B中加入CuO后过滤,这次过滤控制的条件是 。
(4) 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
查看答案和解析>>
科目: 来源: 题型:
(1)25℃时, 0.05mol/LH2SO4溶液的PH=_________;0.05mol/LBa(OH)2溶液C(H+)=____
(2)某温度下纯水中的C(H+)= 2×10-7mol/L,则此时溶液中的C(OH-)= ;若温度不变,滴入稀盐酸,使C(H+)= 5×10-4mol/L,则溶液中C(OH-)= ,此时溶液中由水电离产生的C(H+)= 。
(3)已知100℃时,KW=1×10-12.在该温度下,将100ml0.001 mol/L的NaOH溶液加水稀释至1L,则该溶液的PH为 。
查看答案和解析>>
科目: 来源: 题型:
化学工业在国民经济中占有极其重要的地位,江苏省是国内最早的硫酸生产基地之一。主要方程式和主要设备: (黄铁矿的主要成分为FeS2) 4FeS2+11O2 = 2Fe2O3+8SO2 (沸腾炉) 2SO2+O2![]() 2SO3 (接触室) SO3+H2O=H2SO4(吸收塔)
2SO3 (接触室) SO3+H2O=H2SO4(吸收塔)
(1)硫酸生产中,根据化学平衡原理来确定的条件或措施有 (填写序号)。
A.矿石加入沸腾炉之前先粉碎 B.接触室的反应使用V2O5作催化剂
C.接触室中不使用很高的温度 D.净化后炉气中要有过量的空气
E.接触室中的氧化在常压下进行 F.吸收塔中用98.3%的浓硫酸吸收SO3
(2)0.1mol/L的NaHSO3溶液中,有关粒子浓度由大到小的顺序为:
c (Na+)>c (HSO3-)>c (SO32-)>c (H2SO3)
①该溶液中c (H+) c (OH-)(填“>”、“=” 或“<” ),其理由是(用离子方程式表示): 。
②现向NaHSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是 ,反应的离子方程式为: 。
查看答案和解析>>
科目: 来源: 题型:
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ?mol-1
C3H8(g)+5O2(g) = 3CO2(g) +4H2O(l) △H=-2220.0 kJ?mol-1
根据上面两个热化学方程式回答下列问题:
(1)H2的燃烧热为 .(2)1molH2和2molC3H8 组成的混合气体完全燃烧释放的热量为 。
(3)现有H2和C3H8的混合气体共5mol,完全燃烧时放热3847kJ,则在混合气体中H2和C3H8的体积比是 。
查看答案和解析>>
科目: 来源: 题型:
(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为__ __(填序号)。
A.9 B.13 C.11~13之间 D.9~11之间
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,混合溶液中
c(Na+)___________c(CH3COO-)(填“大于”、“等于”或“小于”)。
(3)如果将HCl和CH3COONa 溶液等浓度、等体积混合,则混合溶液中各离子浓度的大小关系为____________________ ____。
(4) 常温下,若NaOH溶液中的c(OH-)与NH4Cl 溶液中的c(H+)相同,现将NaOH和NH4Cl的溶液分别稀释10倍,稀释后NaOH 和 NH4Cl溶液的pH分别用pH1和pH2表示。则pH1+pH2为 14(可以用“>”、“=”或“<”表示)。
查看答案和解析>>
科目: 来源: 题型:
(1)下图分别是温度计、量筒、滴定管的一部分,则:

量筒应该是 读数为 mL
滴定管应该是 ,读数为 mL
温度计应该是 ,读数是 ℃
(2)用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测量结果偏高的是 。
① 用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡。
②滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失 ③中和滴定时,锥形瓶内有少量蒸馏水。④酸式滴定管用蒸馏水洗后,未用标准液洗。 ⑤读取滴定管终点读数时,仰视刻度线。
查看答案和解析>>
科目: 来源: 题型:
用50 mL0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。
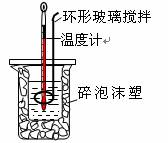
(1)在该实验中,量取50 mL 盐酸或NaOH 溶液,需要用到的玻璃仪器是___________。
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是______________________________。
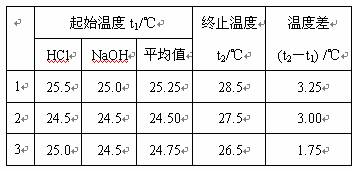
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指__________________温度。
(4)计算该实验发生中和反应时放出的热量为________________kJ(中和后生成的溶液的比热容c=4.18J/(g?℃) ,稀溶液的密度都为1g/cm3)。
(5) 如果用50 mL 0.55mol/L的氨水(NH3?H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是
________________________ 。
查看答案和解析>>
科目: 来源: 题型:
在373K 时,把0.5 mol N2O4气体通入体积为5 L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol?L-1。在60 s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法正确的是( )
A.前2 s,N2O4的平均反应速率为0.01 mol?L-1?s-1
B.在2 s时,体系内压强为反应前的1.1倍
C.平衡时,体系内含NO2 为0.04 mol?L-1
D.平衡时,N2O4的转化率为60%
查看答案和解析>>
科目: 来源: 题型:
二元酸H2A在水中的电离情况是:H2A=H++HA-和HA-![]() H++A2-,则下列物质的水溶液中粒子浓度之间存在的关系错误的是( )
H++A2-,则下列物质的水溶液中粒子浓度之间存在的关系错误的是( )
A.NaHA:c(Na+)>c(HA-)>c(OH-)>c(H+)
B.NaHA:c(Na+)=c(A2-)+c(HA-)+c(H2A)
C.Na2A: c(Na+)>c(A2-)>c(OH-)>c(H+)
D.H2A: c(H+)=c(HA-)+2 c(A2-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com