
科目: 来源: 题型:
氧化还原反应的实质是电子的转移,下列关于氧化还原反应的叙述正确的是( )
A.在氧化还原反应中,有一种元素被氧化,肯定有另一种元素被还原
B.11.2L Cl2通入足量的NaOH溶液中,转移的电子数为0.5NA
C.难失电子的原子,得电子的能力一定强
D.元素由化合态变成游离态时,它可能被氧化,也可能被还原
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列说法不正确的是( )
A.18g水中含有的电子数为10NA
B.46g二氧化氮和46g四氧化二氮含有的原子数均为3NA
C.1L 1mol?L―1的盐酸溶液中,所含氯化氢分子数为NA
D.标准状况下,11.2L臭氧中含1.5NA个氧原子
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是( )
A.由同种元素组成的物质肯定属于纯净物
B.一种元素可形成多种离子,但只能是带同种电荷的离子
C.含金属元素的离子不一定都是阳离子
D.具有相同质子数的粒子都属于同种元素
查看答案和解析>>
科目: 来源: 题型:
2007年10月24日,“嫦娥一号”开始了它的探月历程,它的一项重要任务是探测月球表面土壤里的一种非常有用的资源――可控核聚变的原料3He,3He是一种安全高效而又清洁无污染的物质,据统计,月球上的3He可以满足人类1万年以上的供电需求,月球土壤的3He含量可达500万吨。关于3He的叙述正确的是( )
A.3He和4He两种核素互为同素异形体
B.3He和4He两种核素互为同位素
C.核聚变时,原子核发生了变化,发生了化学反应
D.在3He中存在:质子数=中子数=核外电子数
查看答案和解析>>
科目: 来源: 题型:
2008年夏季奥运会将在我国举行,这次奥运会要突出“绿色奥运、科技奥运、人文奥运”的理念,其中“绿色奥运”是指 ( )
A.把环境保护作为奥运设施规划和建设的首要条件
B.严禁使用兴奋剂,使运动员公平竞争
C.所有奥运用品全是绿色的
D.奥运场馆建设均使用天然材料,不使用合成材料
查看答案和解析>>
科目: 来源: 题型:
1mol气态钠离子和1mol气态氯离子结合生成1mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能。
(1)下列变化过程中,能直接表示出氯化钠晶体格能的是 。
A.Na+(g)+Cl-(g) →NaCl(s);△Q
B.Na(s)+![]() Cl2(g) →NaCl(s);△Q1
Cl2(g) →NaCl(s);△Q1
C.Na(s) →Na(g);△Q2 D.Na(g)-e-→Na+(g);△Q3
E.![]() Cl2(g) → Cl(g);△Q4 F.Cl(g)+e-→ Cl-(g);△Q5
Cl2(g) → Cl(g);△Q4 F.Cl(g)+e-→ Cl-(g);△Q5
(2)写出△Q1与△Q、△Q2、△Q3、△Q4、△Q5之间的关系式 。
(3)若氧化亚铁晶体结构与氯化钠晶体结构相似,则氧化亚铁晶体中,跟二价铁离子紧邻且等距的氧离子个数是 。
(4)若氧化亚铁晶体中有3n个二价铁离子被2n个三价铁离子所替代,该晶体中氧离子的数目将______ (填“减少”、“增多”或“保持不变”)。
查看答案和解析>>
科目: 来源: 题型:
生产工程塑料PBT (![]() ) 的重要原料G(1,4-丁二醇),可以通过下图三种不同的合成路线制备。已知A为乙炔,B的所有原子均处于同一平面上。
) 的重要原料G(1,4-丁二醇),可以通过下图三种不同的合成路线制备。已知A为乙炔,B的所有原子均处于同一平面上。
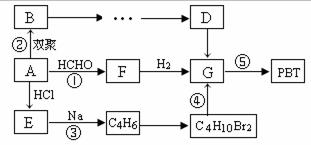
请结合下列所给信息,回答有关问题。
I. CH2=CH-CH=CH2与Br2的CCl4溶液发生1:1加成反应,可得到BrCH2-CH=CH-CH2Br和BrCH2-CHBr-CH=CH2两种产物。
II.2R-Cl + 2Na ![]() R-R + 2NaCl
R-R + 2NaCl
III.R1-C≡C-H+R2-CHO ![]()
![]() (R代表不同烃基或H)
(R代表不同烃基或H)
IV.R-C≡C-(CH2)n-CH=CH2+H2 ![]() R-CH=CH-(CH2)n-CH=CH2(n≥0)
R-CH=CH-(CH2)n-CH=CH2(n≥0)
(1)结构简式:E为_________________;F为___________________。
(2)反应⑤的化学反应方程式为:
____________________________________________________________________。
(3)请设计出自B→…→G的反应流程图(有机物用结构简式表示,须注明反应条件)。
提示:①合成过程中无机试剂任选 ②反应流程图表示方法示例如下:
![]()
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组拟用铜屑、氧化铜的混合物与硫酸、硝酸组成的混酸反应制取CuSO4?5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含有Cu(NO3)2,反应中固体完全溶解,两种酸恰好完全反应。设固体混合物的总质量为240g,其中氧化铜的质量分数为x,试回答下列问题:
(1)所得CuSO4?5H2O晶体的质量y的表达式为: g(用x表示);
(2)若要保证固体全部溶解,混酸恰好反应,则混酸中HNO3、H2SO4的物质的量浓度之比(A): (填“A”的取值范围);
(3)若A=![]() ,反应结束时将所得气体在NaOH溶液中全部转化为NaNO3,至少需要
,反应结束时将所得气体在NaOH溶液中全部转化为NaNO3,至少需要
30%的双氧水________________g(保留一位小数)。
查看答案和解析>>
科目: 来源: 题型:
373K时,某1L密闭容器中发生如下可逆反应:A(g)![]() 22 B(g)。其中物质B的物质的量随时间变化如下图所示,试填空:
22 B(g)。其中物质B的物质的量随时间变化如下图所示,试填空:
(1)已知373K时60s达到平衡,则前60s内A的平均反应速率为 。
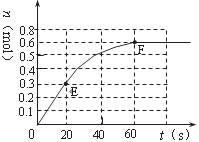
(2)若373K时B的平衡浓度为是A的3倍,473K时(其他条件不变),B的平衡浓度为A的2倍,请在上图中画出473K时A的物质的量随时间的变化曲线。
(3)若反应在373K进行,在1L密闭容器中加入1mol B、0.2molHe,达到平衡时B的转化率是:___________(填序号)。
A.等于60% B.等于40%
C.小于40% D.介于40%~60%之间
(4)已知曲线上任意两点之间连线的斜率表示该时段内B的平均反应速率(例如直线EF的斜率表示20s~60s内B的平均反应速率),试猜想曲线上任意一点的切线斜率的意义
。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F六种物质在一定条件下有下图所示的相互转化关系,所有反应物和生成物均已给出。试回答:
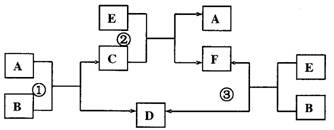
(1)若反应①、②、③均为溶液中的置换反应,A、D、E为常见金属单质,则A、D、E的还原性由强到弱的顺序为____________________。请写出满足以上要求的离子方程式:
反应①________________________________________________________________。
反应②________________________________________________________________。
(2)若反应①、②、③均为复分解反应。且A、E均为常见碱,溶液中形成的D是白色沉淀。请写出满足要求的化学方程式:
反应①________________________________________________________________。
反应②________________________________________________________________。
(3)若B是水,C是一种有磁性的化合物,E是一种无色、无味的有毒气体,则反应①的化学方程式是_____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com