
科目: 来源: 题型:
正确掌握化学用语是学好化学的基础。下列化学用语中正确的是( )
A.乙烯的结构简式为CH2CH2
B.葡萄糖的实验式(最简式)为 C6H12O6 。
C.Ca2+的结构示意图为![]()
D .NH4Cl的电子式为![]()
查看答案和解析>>
科目: 来源: 题型:
2007年诺贝尔化学奖授予德国化学家 GerhardErtl ,以表彰他对固体表面化学过程研究的重大发现。使 CO、NOx等在铂表面发生化学反应转变成无毒气体,以减少汽车尾气中有毒气体的排放,正是此项研究的重要应用之一。下列有关说法不正确的是( )

A.CO能与血红蛋白结合
B.CO、NOx在铂催化作用下反应生成CO2和N2
C.汽车尾气中的CO主要来自汽油的不完全燃烧
D.汽车尾气中的NOx主要来自汽油中含氮化合物的燃烧
查看答案和解析>>
科目: 来源: 题型:
碱式碳酸镁和无水氯化镁具有广泛的用途。
●用白云石(CaCO3?MgCO3)为主要原料生产碱式碳酸镁和无水氯化镁的流程如下:
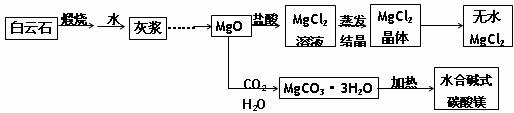
回答下列问题:
(1)“灰浆”中除水和MgO处,主要成分还有:_____________。
(2)从MgCl2晶体得到无水MgCl2的操作为:________________。
●为探究所制得的水合碱式碳酸镁(mMgCO3?nMg(OH)2?xH2O)的组成,某同学组装仪器如图所示:
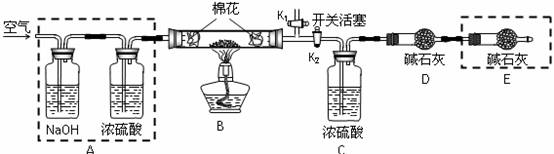 (3)实验测得:硬质玻璃管中剩余的固体质量为1.60g,C处浓H2SO4增重0.72g,D处碱石灰增重1.32g,则此水合碱式碳酸镁的化学式为:______________。
(3)实验测得:硬质玻璃管中剩余的固体质量为1.60g,C处浓H2SO4增重0.72g,D处碱石灰增重1.32g,则此水合碱式碳酸镁的化学式为:______________。
(4)A框中装置的作用是______________;在装好试剂后,加热前应进行的操作是_____。
(5)若将E框中的装置去掉,对实验结果的影响是_______________________。
查看答案和解析>>
科目: 来源: 题型:
下表列有几种物质的沸点:
⑴
| 物质 | AlF3 | AlCl3 | AlBr3 | Al2O3 | MgCl2 | MgO |
| 沸点/℃ | 1260 | 181(升华) | 263 | 2045 | 707 | 2850 |
①下列各组物质中,气化或者熔化时所克服的粒子间作用力类型分别与氟化铝和溴化铝相同的是 。
A.NaCl和CCl4 B.Na2O和SiO2
C.金刚石和金属铝 D.碘和干冰
②工业上制备金属镁,应采用电解熔融的 。
A.MgCl2 B.MgO
③工业上制备金属铝,是采用电解熔融Al2O3(加冰晶石),而不是电解熔融AlCl3,原因是 。
⑵过渡元素钴(27Co)的原子核外电子排布式为 。钴有两种化学式均为Co(NH3)2BrSO4的配合物,且配位数均为6。它们分别溶解于水时电离出的阳离子的化学式可能为 和 。鉴别两者的实验方法是:分别取样并滴加 (填化学式)溶液.
查看答案和解析>>
科目: 来源: 题型:
乙烯是石油化工的重要原料,它主要通过石油产品裂解获得。
(1)石油产品裂解所得裂解气的平均组成可表示为CnHm(m>2n),经测定某裂解气中各气体的体积分数分别为:甲烷―4%、乙烯―50%、丙烯―10%、其余为丁二烯和氢气(气体体积均在同温同压下测定)。若得到50 mol乙烯,x mol丁二烯和y mol氢气。则x+y= , n / m = (请用含x的式子表示)。
(2)某化工厂每天由石油产品裂解得到乙烯56 t。再以乙烯为主要原料生产醋酸乙烯酯,醋酸乙烯酯是合成维尼纶的重要单体。生产原理如下:
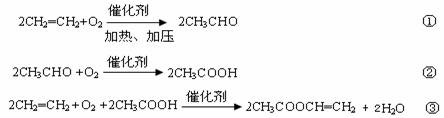
反应①中乙烯的利用率为80%,反应②中乙醛的利用率为83.33%,反应③中乙酸与乙烯的利用率均为85%。则该厂每天最多可制得醋酸乙烯酯多少吨?
查看答案和解析>>
科目: 来源: 题型:
有机物A的结构简式如下图所示:

有机物A在稀硫酸中受热会水解成B、C两种产物,B是一种离子化合物,C是一种共价化合物。
(1)A的分子式为 。在A的结构简式中虚线框内的结构名称为
。
(2)写出C跟碳酸氢钠反应的化学方程式 。
(3)C的同分异构体中,属于酚类也属于酯类的化合物有 种。
(4)某类有机物,属于C的同分异构体,分子中有苯环且苯环上连有三个取代基。写出这类有机物的结构简式 ,其中含氧官能团的名称 。
查看答案和解析>>
科目: 来源: 题型:
目前有科学家在一定条件下利用水煤气(CO+H2)合成甲醇:
CO(g)+2H2(g)![]() CH3OH(g)。甲醇的物质的量与反应温度的关系如下图所示:
CH3OH(g)。甲醇的物质的量与反应温度的关系如下图所示:

①合成甲醇反应,其反应热△H______0。(填“>”、“<”或“=”)
②其它条件不变,对处于E点的体系体积压缩到原来的1/2,正反应速率加快,逆反应速率_________。(填“加快”、“减慢”、“不变”)重新平衡时c(CH3OH)/c(CO)_________。(填“增大”、“减小”或“不变”)
③据研究,合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)_______________________________________。
查看答案和解析>>
科目: 来源: 题型:
利用核能把水分解制氢气,是目前正在研究的课题。下图是其中的一种流程,其中用了过量的碘。
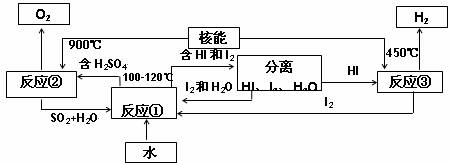
完成下列反应的化学方程式:反应①______________;反应②________________________。此法制取氢气的最大优点是_____________________________。
查看答案和解析>>
科目: 来源: 题型:
某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤
①CaBr2+H2O![]() CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg![]() HgBr2+H2
HgBr2+H2
③HgBr2+_____![]() _____ ④2HgO
_____ ④2HgO![]() 2Hg+O2↑
2Hg+O2↑
⑤2H2 +O2![]() 2H2O
2H2O
请你根据“原子经济”的思想完成上述步骤③的化学方程式:______________。并根据“绿色化学”的思想评估该方法制H2的主要缺点:__________________。
查看答案和解析>>
科目: 来源: 题型:
“氢能”将是未来最理想的新能源。实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为___________________________。(填序号)
A.2H2(g)+O2(g) ![]() 2H2O(l); △H=-142.9kJ?mol―1
2H2O(l); △H=-142.9kJ?mol―1
B.H2(g)+![]() O2(g)
O2(g) ![]() H2O(l); △H=-285.8kJ?mol―1
H2O(l); △H=-285.8kJ?mol―1
C.2H2+O2![]() 2H2O(l); △H=-571.6kJ?mol―1
2H2O(l); △H=-571.6kJ?mol―1
D.H2(g)+![]() O2(g)
O2(g) ![]() H2O(g); △H=-285.8kJ?mol―1
H2O(g); △H=-285.8kJ?mol―1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com