
科目: 来源: 题型:
某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠含量,设计了三种实验方案,请结合以下方案回答有关问题:
方案一:称取一定量的氢氧化钠样品mlg ,加水溶解后,逐滴加入沉淀剂至不再产生沉淀为止。将沉淀过滤、洗涤、干燥、称量其质量为 m2g。沉淀剂使用氢氧化钡溶液而不用氢氧化钙溶液,结果将具有更高的精确度,原因是
方案二:利用下图装置测定氢氧化钠样品中 Na2CO3的含量。计算Na2CO3质量分数时,必需测定的数据是
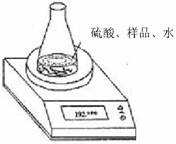
方案三:操作流程如下:
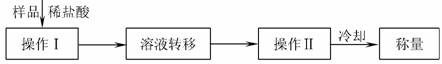
需直接测定的数据是 ;在转移溶液时,如溶液转移不完全,则Na2CO3质量分数的测定结果 (填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
铜合金是人类使用最早的金属材料。铜在化合物中的常见化合价有+l、 +2 等,故能形成多种铜的化合物。
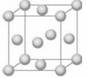
(1)基态 Cu 原子的电子排布式是 ;铜晶体晶胞如图所示,该晶胞实际拥有 个铜原子;
(2)①某+ l 价铜的配离子为[Cu(CN)4]3-,与配体互为等电子体的一种微粒是 (写化学式)。
②许多+l价铜的配合物溶液能吸收CO和烯烃(如C2H4、CH3CH= CH 2等), CH3CH= CH 2分子中c子采取的杂化方式有 。
(3)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液。写出此蓝色沉淀溶解的离子方程式: ;根据价层电子对互斥模型,预测SO42一的空间构型为 。
查看答案和解析>>
科目: 来源: 题型:
超细硅酸铝具有极好的悬浮性和纯白外观,与颜料配合能明显地改进涂料的白度。其样品化学式可表示为AlxSi35Oy?ZH2O企业标准规定超细硅酸铝中含水量7%~10%为优良级。某化学兴趣小组为测定该样品的组成,按如下步骤处理:
步骤一:准确称取 9.936g 超细硅酸铝样品,充分加热至不再分解为止,冷却、称量,得固体9.216g 。
步骤二:另准确称取 9.936g 超细硅酸铝样品,加足量盐酸,充分反应后,过滤,洗涤,烘干得SiO2固体 8.400g。
(1)计算该超细硅酸铝样品是否为优良级。
(2)求该样品的化学式。
查看答案和解析>>
科目: 来源: 题型:
氯霉素是广普抑菌抗生素。下图是以乙苯为原料合成氯霉素的合成路线。

已知:
在稀碱催化下,一些含羰基的化合物能发生如下反应:

试回答下列问题:
(1)上述转化(①、②、③、④)中,属于取代反应的有(填序号,下同) ;属于氧化反应的有 ;属于加成反应的有 。
(2)试剂A的结构简式为 ;
(3)有机物![]() 的同分异构体甚多。其中含有―NO2、―CHO、―CH3、
的同分异构体甚多。其中含有―NO2、―CHO、―CH3、![]() 四种基团的同分异构体共有6种,结构简式为
四种基团的同分异构体共有6种,结构简式为
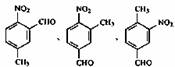 、 、 ;
、 、 ;
(4)写出中间体B在盐酸作用下发生水解的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下:
(I)将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液。
(II)将电解饱和食盐水所得气体反应后制得盐酸。
(III)将盐酸加入NaHSO3溶液中得SO2气体回收,生成的NaCl循环利用。
①写出步骤(I)反应的化学方程式: ;
②写出步骤(III)反应的离子方程式: ;
(2)某研究性学习小组采用下图装置在实验室测定废气样品(含SO2、O2、N2、CO2等)中SO2的体积分数,X溶液可能是 ;
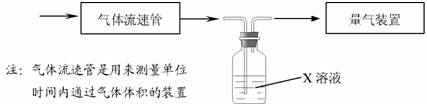
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.氯化钡溶液
查看答案和解析>>
科目: 来源: 题型:
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)实验测得,在通常情况下,1gH2完全燃烧生成液态水,放出 142 . 9 kJ 热量。则H2燃烧的热化学方程式为
(2)用氢氧燃料电池进行下图所示实验。
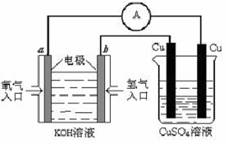
①氢氧燃料电池中,正极的电极反应式为
②上图装置中,某一铜电极的质量减轻3.2g,则a极上消耗的O2在标准状况下的体积
为 L
(3)用氢气是合成氨,反应的热化学方程式如下:
N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4KJ/mol
2NH3(g) △H=-92.4KJ/mol
① 下图表示合成氨反应达到平衡后,每次只改变温度、压强、催化剂中的某一条件,反应速率v与时间t的关系。其中表示平衡混合物中的NH3的含量最高的一段时间是 。图中t3时改变的条件可能是 。

②温度为T℃时,将4amolH2和2amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50。则反应的平衡常数为 。
查看答案和解析>>
科目: 来源: 题型:
中学化学中几种常见物质的转化关系如下图所示(部分反应物、生成物及反应条件已略去):
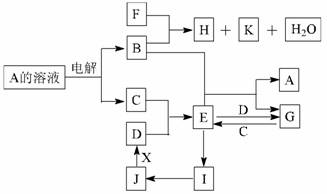
已知:B、C、D为常见单质,其中C为气体,B、D为金属;F为常见的强酸;K常温下为气体,且能使品红溶液褪色;将E的饱和溶液滴入沸水可制得一种红褐色胶体; J为红棕色固体。请回答下列问题:
(1)C的化学式为 ;
写出B与F反应的化学方程式
(2)实验中保存G溶液时要加入 目的是
(3)为实现J→D的变化,若X是非金属单质,则X可能是 (写化学式);若X是金属单质,请写出 J→D 反应的化学方程式
查看答案和解析>>
科目: 来源: 题型:
实验室可以通过三条途径来制取N2:
①加热条件下用NH3还原CuO制得纯净的N2和铜粉,反应的化学方程式为:
![]()
② 将空气通过灼热的铜粉制得的N2
③ 加热NaNO2(有毒性)与NH4Cl的混合浓溶液制取N2,反应的化学方程式为:
![]()
按上述途径制N2可供选择的实验仪器如下图所示,其他必要的仪器如铁架台、铁夹、铁圈、石棉网、酒精灯等未列出。
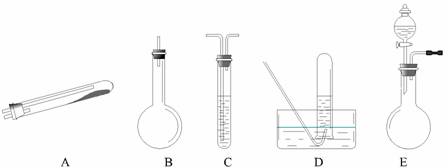
(1)按途径 ① 制取N2时所需的氨气要用浓氨水与生石灰反应得到,化学方程式为:
CaO+NH3?H2O === Ca(OH)2+NH3↑,,最好要用上述装置中的 。 (填字母,下同)作为氨气发生装置。要制取并收集N2,还应使用到上述装置中的
(2)①和②两种途径常常被联合使用。这种方法与途径③相比其优越性在于 。
(3)检查E装置气密性的方法是 。利用E装置还可以制取的气体有 (只需写出三种)。
查看答案和解析>>
科目: 来源: 题型:
向1 . 00 L0.3mol / L 的NaOH 溶液中缓慢通入8.8gCO2气体,使其完全反应,对反应后的溶液,下列判断正确的是 ( )
A.溶质为Na2CO3
B.溶质为NaHCO3
C.![]() c(Na+) = c(HCO-3)+c(CO2-3)+c(H2CO3)
c(Na+) = c(HCO-3)+c(CO2-3)+c(H2CO3)
D.c(Na+)+c(H+) = c(HCO-3) + 2c(CO2-3)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
根据下图判断,下列说法正确的是( )

A.若反应I中的△H<0,则T2 > T1
B.若反应I中的△H>0,则T2 < T1
C.反应II的平衡不受压强的影响
D.若反应II中的△H>0,则T2 < T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com