
科目: 来源: 题型:
下列离子方程式中正确的是( )
A.Fe3O4与稀HNO3反应:Fe3O4+8H+==Fe2++2Fe3++4H2O
B.Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+2OH-=CaCO3↓+ CO32-+2H2O
C.Na2CO3溶液中通入少量CO2::CO32-+ CO2+ H2O=2HCO3-
D.F2与NaOH溶液反应:F2+4OH-==2F-+O2+2H2O
查看答案和解析>>
科目: 来源: 题型:
氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
A.一个D2O分子所含的中子数为8
B.NH3的结构式为![]()
C.HCl的电子式为![]()
D.热稳定性:H2S>HF
查看答案和解析>>
科目: 来源: 题型:
闪电时空气中有臭氧生成。下列说法中正确的是( )
A.O3和O2互为同位素
B.O2比O3稳定
C.等体积O3和O2含有相同质子数
D.O3与O2的相互转化是物理变化
查看答案和解析>>
科目: 来源: 题型:
NA为阿伏加德罗常数,下列正确的是……( )
A、80g硝铵含有氮原子数为2NA
B、1L1mol?L-1的盐酸溶液中,所含氯化氢分子数为NA
C、标准状况下,11.2L四氯化碳所含分子数为0.5NA
D、在铜与硫的反应中,1mol铜失去的电子数为2NA
查看答案和解析>>
科目: 来源: 题型:
下列两种溶液反应,将第一种溶液滴入第二种溶液与将第二种溶液滴入第一种溶液时发生反应不完全相同的是( )
①AlCl3与NaOH ②AgNO3与氨水③Na3PO4与H2SO4 ④NaAlO2与盐酸 ⑤苯酚钠与盐酸
A、①②⑤ B、①②③④ C、②③⑤ D、全部
查看答案和解析>>
科目: 来源: 题型:阅读理解
为测定碳酸钙纯度(设含杂质SiO2),学生设计了如下几个实验方案,请回答每个方案中的问题。
[方案I] (1)称取碳酸钙样品M g;
(2)加入过量盐酸;
(3)收集并测定生成的气体体积 V mL。
问题:如果称量样品时,砝码底部有一处未被实验者发现的残缺,那么测定的碳酸钙的纯度会 (偏高、偏低、无影响)
[方案II](1)称取碳酸钙样品 M g;
(2)用c mol/L 盐酸 V mL(过量)溶解样品;
(3)取溶解后的溶液![]() mL,用C′mol/L NaOH溶液滴定,恰好用去V′mL。
mL,用C′mol/L NaOH溶液滴定,恰好用去V′mL。
问题1:列出本实验中所用到的仪器名称(除铁架台及附件、烧杯之外)
。
问题2:加盐酸后是否需要滤出SiO2后再用NaOH滴定 (填选项编号)。
A.需要 B.不需要 C.均可
问题3:碳酸钙纯度计算公式 。
[方案III](1)称取碳酸钙样品 M g;
(2)高温(1000℃)煅烧直至质量不再发生变化,冷却后称量,质量为M′g。
问题1:为什么要煅烧至1000℃且“直至质量不再改变”? ;
问题2:本方案中的“冷却”应如何操作 。
[方案IV](1)称取碳酸钙样品 M g;
(2)加入足量Cmol/L盐酸V mL使之完全溶解;
(3)过滤并取滤液;
(4)在滤液中加入过量C′mol/L Na2CO3溶液V′mL;
(5)将步骤(4)中的沉淀滤出、洗涤、干燥、称重为M′g。
问题1:此方案中不需要的数据是 (填选项编号)。
A.C、V B.C′、 V′ C. M′ D. M
问题2:为减少实验误差,必要的操作是 (填选项编号)。
A.精确测定Na2CO3溶液体积V′ mL
B.精确配制浓度C′mol/LNa2CO3溶液
C.将步骤(3)所得沉淀洗涤,洗涤液也应并入(4)中
D.将步骤(3)所得沉淀洗涤、干燥、称量其质量M′g备用
问题3:步骤(5)中要将沉淀进行洗涤,如果未经洗涤,则测定的碳酸钙纯度将 (偏高、偏低、无影响)。
综上所述,你认为4个方案中,最好的方案是 ,其它方案的缺点分别是:
方案IV:沉淀的洗涤、干燥、称量操作过程复杂,容易造成较大误差;
方案 ; 。
方案 ; 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如下图。某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为完全正确(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项 。

| 序号 | 猜想物质的化学式 | 检验需要的试剂 | 操作、现象及结论 |
| A | Na2SO4 | 稀盐酸、氯化钡溶液 | 取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4。 |
| B | Na2CO3 | 稀盐酸、澄清的石灰水、品红溶液 | 取少量该溶液于试管中,滴入稀盐酸,如果产生的气体不能使品红溶液褪色而能使澄清的石灰水变浑浊,则原溶液是 Na2CO3。 |
| C | Na2SO3 | 稀盐酸、澄清的石灰水 | 取少量该溶液于试管中,滴入稀盐酸,如果产生无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2SO3。 |
| D | Na2SiO3 | 过量稀盐酸 | 取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀溶解,则原溶液是Na2SiO3溶液。 |
| E | Na2S2O3 | 稀盐酸 | 取少量该溶液于试管中,滴入稀盐酸,如果溶液变浑浊(或产生淡黄色沉淀),并产生无色有剌激性气味的气体,则原溶液是Na2S2O3溶液。 |
除上述五种可能之外,写出你认为还有可能物质的化学式(1种): 。
查看答案和解析>>
科目: 来源: 题型:
A~J是中学化学中常见的几种物质,它们之间的转化关系如下图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作禽流感、SARS等病毒的杀菌消毒剂。
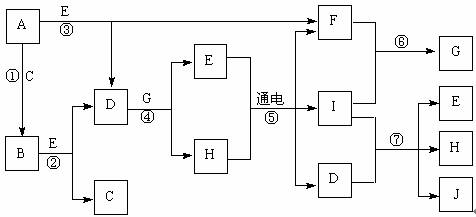
(1)写出E、B的电子式:B_______________。E_____________。
(2)写出反应⑦的离子方程式:_________________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:____________。
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:_______。_____极(填“阴”或“阳”)附近溶液由无色变为红色。
查看答案和解析>>
科目: 来源: 题型:
能源是人类社会发展进步的物质基础。在当代,能源同信息、材料一起构成了现代文明的三大支柱。
(1)为了降低汽车尾气对大气的污染,江苏有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。请写出表示甲醇燃烧热的热化学方程式。
(2)测定工业甲醇中CH3OH的质量分数可按下法:取0.1000g工业甲醇样品,以适量H2SO4酸化后,加入20.00mL 0.2000mol/L的K2Cr2O7溶液,再用0.3000mol/L (NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00mL时,刚好到达滴定终点。
已知:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式。
②此工业甲醇中CH3OH的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com