
科目: 来源: 题型:
纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,其总反应式为:( )
![]() 下列说法正确的是
下列说法正确的是
A.放电时,溶液中![]() 向正极移动,
向正极移动,![]() 向负极移动
向负极移动
B.放电时,正极反应式为:![]()
C.在电池放电过程中,电解质溶液的酸碱性保持不变
D.放电时,锌是负极,发生还原反应,电极反应式为:![]()
查看答案和解析>>
科目: 来源: 题型:
呋喃西林属于硝基呋喃类抗生素,曾作为广谱抗菌药,在动物养殖中发挥杀菌防腐 作用。但后来发现具有致突变和致癌作用。2002年4月,农业部规定,硝基呋喃类化合物禁止用于所有食品动物。呋喃西林的结构简式是: ( )
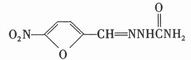
下列说法正确的是
A. 呋喃西林中含有苯环 B.呋喃西林的化学式为![]()
C.呋喃西林的摩尔质量为198 D.呋喃西林不能发生加成反应
查看答案和解析>>
科目: 来源: 题型:
有一瓶五色溶液,可能含有![]() 离子中的几种。为确定其成分,做了如下实验:①取部分溶液,加入适量
离子中的几种。为确定其成分,做了如下实验:①取部分溶液,加入适量![]() 固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入
固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入![]() 酸化的
酸化的![]() 溶液,有白色沉淀产生。下列推断正确的是 ( )
溶液,有白色沉淀产生。下列推断正确的是 ( )
A.肯定有![]() B.肯定有
B.肯定有![]()
C.肯定有![]() D.肯定有
D.肯定有![]()
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,正确的是 ( )
①根据![]() 分子结构可推知,COS分子中各原子也达到了8电子结构 ②将
分子结构可推知,COS分子中各原子也达到了8电子结构 ②将![]() 溶液加热蒸发至干并灼烧,最后得到红棕色粉末 ③向
溶液加热蒸发至干并灼烧,最后得到红棕色粉末 ③向![]() 溶液中滴加
溶液中滴加![]() 溶液至刚好沉淀完全的离子方程为:
溶液至刚好沉淀完全的离子方程为:
![]()
④NaHS溶液中,![]() 水解的离子方程式为:
水解的离子方程式为:![]()
⑤![]() 结合
结合![]() 的能力比
的能力比![]() 的强
的强
A.②④⑤ B.①②③ C.①③④ D.①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
![]() 表示阿伏加德罗常数的值,下列说法正确的是 ( )
表示阿伏加德罗常数的值,下列说法正确的是 ( )
A. 1mol羟基(-OH)中所含电子数为7![]()
B.实验室中用含4molHCl的浓盐酸跟足量![]() 反应,可制得
反应,可制得![]() 的分子数为
的分子数为![]()
C.常温常压下,1mol ![]() 和NO的混合气体中含有的原子数为2
和NO的混合气体中含有的原子数为2![]()
D.标准状况下,22.4L![]() 中所含原子数为4
中所含原子数为4![]()
查看答案和解析>>
科目: 来源: 题型:
据报道,碳纳米管是碳原子形成的大分子,其导电性是铜的1万倍;![]() 是可用作烈性炸药的一种分子,下列说法正确的是 ( )
是可用作烈性炸药的一种分子,下列说法正确的是 ( )
A.金刚石与碳纳米管互为同分异构体
B.![]() 与
与![]() 互为同素异形体
互为同素异形体
C.![]() 的中子数和
的中子数和![]() 的质子数相等
的质子数相等
D.C原子半径比N原子半径小
查看答案和解析>>
科目: 来源: 题型:
M5纤维是美国开发的一种超高性能纤维,据报道,美国士兵佩带的头盔、防弹背心和刚性
前后防护板中含有M5纤维。M5纤维是刚杆形又有强力分子间氢键的聚合物。下面是M5纤维的合成线路:(有些反应未注明条件)

请填写下列空白:
(1)合成M5的单体的结构简式F._______________,G.___________________;
(2)反应类型:A→B:________________;B→C:________________ :
(3)在生成A的反应中,对二甲苯与氯气按物质的量之比1:2发生反应,生成A的同时 可能生成的A的同分异构体 _________________。(写结构简式);
(4)写出化学反应方程式:C→对苯二甲酸:________________________。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为![]() ,B元素的原子价电子排布为
,B元素的原子价电子排布为![]() ,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P亚层中有3个电子。
,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P亚层中有3个电子。
(1)C原子的电子排布式为_______,若A元素的原子最外层电子排布为![]() ,则按原子轨道的重迭方式,A与C形成的化合物中的共价键属于__________键。
,则按原子轨道的重迭方式,A与C形成的化合物中的共价键属于__________键。
(2)当n=2时,B的原子结构示意图为_______,B与C形成的晶体属于_______晶体。
当n=3时,B与C形成的晶体中微粒间的作用力是_______________。
(3)若A元素的原子最外层电子排布为![]() ,B元素的原子价电子排布为
,B元素的原子价电子排布为![]() ,元素A在周期表中的位置是__________,A、B、C、D四种元素的第一电离能由大到小的顺序是 __________(用元素符号表示)。
,元素A在周期表中的位置是__________,A、B、C、D四种元素的第一电离能由大到小的顺序是 __________(用元素符号表示)。
查看答案和解析>>
科目: 来源: 题型:
氢氧化钠是一种用途十分广泛的重要化工原料。工业上主要通过电解氯化钠饱和溶液的方法获得氢氧化钠,我国的氯碱工业大多采用离子交换膜电解槽。
(1)离子交换膜电解槽一般采用金属钛作阳极,其原因是____________________________。
阴极一般用碳钢网制成。阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是_______.
(2)为使电解氯化钠的速度加快,下列措施中,可行的是_____________________。
A.增大阴极碳钢网面积 B.提高饱和氯化钠溶液的温度
C.加大阴极与阳极间的距离 D.提高电解时的电源电压
(3)如果将某离子交换膜电解槽有关条件进行如下改变,则能使电解速率一定会达到原来的2倍的是____________。
①电解时的电压增大到原来的2倍
②电解时的电流增大到原来的2倍
③电解时的温度从30℃提高到60℃
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件及部分产物未标出)。

(1)若A、D、F都是非金属单质,常温下,A、D为固体,D单质可作为半导体材料,F为气体,且A、D所含元素为同主族短周期元素,A、F所含元素同周期,则反应①的化学方程式是___________________________。
(2)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,C的溶液为浅绿色,则反应②(在水溶液中进行)的离子方程式是:_____________________________;已知1gD与足量F在光照的条件下完全反应生成B时,放出92.3 kJ热量,试写出该反应的热化学方程式:_______________。工业上可用电解方法同时制得D和F,写出电解过程中阳极的电极反应式:________________________________________.
(3)若B、C、F都是气态单质,且B有毒呈黄绿色,反应③中有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则反应③的化学方程式是_________________。
(4)若A、B、D为有机物,B的相对分子质量比A大14,E、F为无机物单质,C为最常见的氧化物,通常状况下为液态,C能与乙烯在一定条件下发生加成反应生成A。则E的化学式为_______________,D的结构简式为______________,反应①属于__________反应,反应③的化学方程式为_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com