
科目: 来源: 题型:
下列各组物质的稀溶液发生反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是 ( )
A.NaHSO4和Ba(OH)2 B.AlCl3和NaOH
C.NaAlO2 和H2SO4 D.Ba(HCO3)2 和Ba(OH)2
查看答案和解析>>
科目: 来源: 题型:
钡和钠相似,也能形成含O22-离子的过氧化物,下列叙述不正确的是 ( )
A.过氧化钡的化学式是Ba2O2
B.1 mol过氧化钡或过氧化钠跟足量的水反应都生成0.5 mol氧气
C.O22-离子的电子式为![]()
D.过氧化钡或过氯化钠都是强氧化剂
查看答案和解析>>
科目: 来源: 题型:
有X、Y、Z三种元素,已知:
①X2-、Y―均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色。
请回答:
(1)Y的最高价氧化物对应水化物的化学式是______________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是___________,
此液体具有的性质是___________(填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通过直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1 mol该气体被O2氧化放热98.0 kJ。若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为___________。
②原无色有刺激性气味的气体与含1.5 mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若1.5×6.02×10![]() 个电子转移时,该反应的化学方程式是___________。
个电子转移时,该反应的化学方程式是___________。
查看答案和解析>>
科目: 来源: 题型:
根据测定硫酸铜晶体中结晶水含量的实验,填写下列空白:
⑴ 有下列仪器,本实验中需要的仪器是(填写字母)__________,
除上述仪器外,还需要的仪器是(填仪器名称):____________。
A、带砝码的托盘天平 B、研钵 C、试管夹 D、酒精灯 E、蒸发皿
F、玻璃棒 G、坩埚 H、干燥管 I、石棉网 J、三角架
⑵ 本实验至少需要加热_____________次,至少需要称量__________次;
⑶ 某学生实验得到以下数据:加热前容器的质量为m1,容器和晶体的总质量为m2,加热后容器和无水CuSO4的总质量为m3。请写出结晶水含量(ω)的计算公式并求出CuSO4?nH2O中n的值(用ml、m2、m3表示):ω= _______________,n = _________________
⑷ 若ml = 5.4g、m2 = 7.9g、m3 = 6.8g,该生测得实验结果偏高还是偏低? _______________
从下列分析中选出该生实验产生误差的原因可能是(填写字母) ___________________
A、加热前称量时容器未完全干燥
B、最后两次加热后的质量差大于0.1g
C、加热后容器未放在干燥容器中冷却
D、加热过程中有少量晶体溅出
E、加热后的粉末中有少量黑色固体
查看答案和解析>>
科目: 来源: 题型:
下列实验操作或对实验事实的叙述正确的是__________(填序号)
① 为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴CuSO4溶液;
② 向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
③ 使用胶头滴管的任何实验都不允许将滴管插入液面以下;
④ 为了获得胆矾晶体,可将CuSO4溶液蒸干、灼烧到质量不再发生变化时为止;
⑤ 不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥ 用石英坩埚高温熔融NaOH和Na2CO3的固体混合物;
⑦ 配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
⑧ 用洁净的玻璃棒蘸取稀硫酸,点在pH试纸中部以测定此稀硫酸的pH。
查看答案和解析>>
科目: 来源: 题型:
有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有 (选填序号)。
① 加成反应 ② 酯化反应 ③ 加聚反应 ④ 氧化反应
(2)B分子所含官能团的名称是 、 。
(3)B分子中没有支链,其结构简式是 ,B的具有相同官能团的同分异构体的结构简式是 。
(4)由B制取A的化学方程式是: 。
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
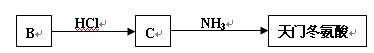
天门冬氨酸的结构简式是 。
查看答案和解析>>
科目: 来源: 题型:
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能 / kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
 请回答下列问题:
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)
SiC_______Si;SiCl4_________SiO2
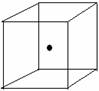
(2)右图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“×”
表示出与之紧邻的硅原子。
(3)工业上用高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)
Si(s)+4HCl(g)
该反应的反应热△H=_____kJ / mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com