
科目: 来源: 题型:
Cu―Fe合金由于长时间置于空气中,表面产生了一怪氧化膜(成份为Fe2O3和CuO),现进行如下实验(以下气体体积均在标况下测得):
①将此合金块5.76g置于烧杯中,然后将稀H2SO4逐渐缓慢加入至过量,收集产生的气体为672mL,过滤得浅绿色溶液A,还有滤渣B。
②将滤渣B投入到一定浓度的HNO3中,完全溶解,得NO、NO2的混合气体896mL,经测定,同温同压下此混合气体对氢气的相对密度为17。
③将①中所得滤液加入到同浓度足量的HNO3中,用排水法收集一烧瓶气体,再向烧瓶中通入224mL O2,气体恰好完全溶于水。
(1)A中存在的阳离子有 、 。
(2)B的单质为 ,质量为 g。
(3)③中被HNO3氧化了的阳离子的物质的量为 mol。
(4)此合金块中氧元素的质量为 g。
查看答案和解析>>
科目: 来源: 题型:
某食盐样品中混有NaBr杂质,为了测定该食盐样品的纯度,可设计实验过程如图甲所示:
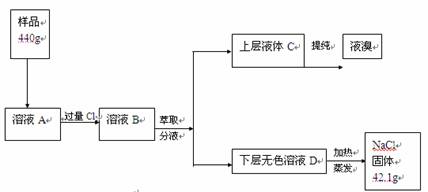
甲图
阅读上述实验过程,完成下列填空:
(1)请你从乙图中选出四个装置(可重复使用),来完成向溶液A中通入过量Cl2的实验,将所选装置的选项字母填入方框,并在括号中写出装置内所放的化学药品。
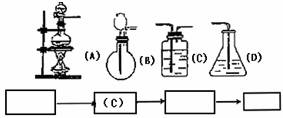
乙图
( ) (饱和食盐水)(溶液A) ( )
(2)为了证明溶液D中几乎不存在Br-,可选用的试剂为(多选不给分) __ 。(填选项字母)
A.碘水 B.淀粉碘化钾溶液
C.新制氯水和四氯化碳 D.食盐水
(3)依据甲图所示,在萃取操作中应选取的有机溶剂为(多选不给分) 。
A.四氯化碳 B.甲苯 C.乙醇 D.裂化汽油
(4)在萃取、分液的过程中,把分液漏斗玻璃塞上的凹槽对漏斗口上的小孔,其目的是 。如丙图所示,待分液漏斗内的混合液分层后,应采取的分离操作是 。
(5)加热蒸发溶液D时,除需带铁圈的铁架台、坩埚钳和火柴外,还必须用到的仪器有 、 、 。
(6)试计算原固体混合物中氯化钠的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
已知:下图中B、G为常见金属单质A、J为非金属气体单质,其余为常见物质或其水溶液,其中E为蓝色沉淀,B在A气体中燃烧产生棕色烟,I的焰色反应为黄色,F为无色气体,遇空气后变为红棕色。
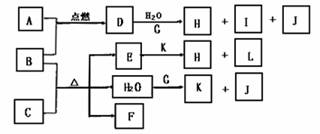
回答下列问题:
(1)写出:①D化学式 ,其水溶液显 性,试用离子方程式说明原因: 。
②K物质中所含的化学键有 ,其中电子式为 。
(2)写出B与C反应的离子方程式 。
(3)1molG与足量的水反应,生成还原产物的质量为 g。
(4)J与另一种常见的无色气体单质在K溶液中可构成一种燃料电池,写出该电池负极的电极反应式________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2mol Cu(OH)2,恰好恢复到电解前的浓度和pH。则电解过程中转移电子的总物质的量为( )
A.0.2mol B.0.4mol C.0.6mol D.0.8mol
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是 ( )
A.0.1mol/L 的Na2CO3溶液中:c(OH-)= c (H+)+ c (HCO![]() )+2 c (H2CO3)
)+2 c (H2CO3)
B.分别取等体积等pH的CH3COOH和HCl,都稀释相同的倍数后测pH,CH3COOH 的pH变化小
C.取等体积等物质的量浓度的CH3COOH和HCl,分别加入相同的Zn粒,比较反应速率,CH3COOH与Zn反应慢
D.溶质为NaOH和CH3COONa的混合液中,离子浓度的关系一定有: c(Na+)> c (OH-)> c (CH3COO-)> c (H+)
查看答案和解析>>
科目: 来源: 题型:
下列有关化学反应的描述正确的是( )
A.将足量稀盐酸加到Mg、AlCl3、NaAlO2组成的固体混合物中,只能发生一种反应
B.把盛有等物质的量的一氧化氮和二氧化氮的混合气体的试管倒置于水槽中,最后剩 余气体理论上为原来气体体积的2/3
C.稀硝酸与铁反应时产物与反应物的量有关,当n(Fe):n(HNO3)≥3:8时产物为Fe3+
D.甘氨酸和(NH4)2S都既能与盐酸反应,又能与NaOH溶液反应且都有气体生成
查看答案和解析>>
科目: 来源: 题型:
对于反应2SO2(g)+O2(g) ![]() 2SO3(g);△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是( )
2SO3(g);△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是( )
(0~t1;v正=v逆;t1时改变条件,t2时重新建立平衡。)

A.增加氧气的浓度 B.增大压强 C.升高温度 D.加入催化剂
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是( )
A.等物质的量浓度的FeBr2和CuCl2混合溶液用惰性电极电解,最初发生:Fe2++2Cl- Fe+Cl2↑
B.硫酸亚铁加入到过氧化氢溶液中:Fe2++H2O2+2H+=Fe3++4H2O
C.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液:
Ca2++2HCO![]() +2OH-=CaCO3↓+2H2O+CO
+2OH-=CaCO3↓+2H2O+CO![]()
D.氯酸钾与浓盐酸制取少量氯气:6H++ClO![]() +5Cl-
+5Cl- 3Cl2↑+3H2O
查看答案和解析>>
科目: 来源: 题型:
若NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.常温常压下,22.4LN2和NO的混合气体所含的原子数为2NA
B.在反应CaO+3C CaC2+CO↑中,生成1 mol CO,转移的电子数为3NA
C.在10.6g Na2CO3晶体中,Na+和CO![]() 的数目比为2:1
的数目比为2:1
D.1mol NH![]() 中含电子数为9NA
中含电子数为9NA
查看答案和解析>>
科目: 来源: 题型:
下列有关叙述中正确的是( )
A.胶体产生丁达尔效应是由胶粒的大小决定的
B.同一主族元素的氢化物,相对分子质量越大,它的沸点一定越高
C.分子晶体溶于水时,一定不破坏共价键
D.同位素的质量数不同,物理性质不同,同位素的不同原子构成的单质化学性质也不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com