
科目: 来源: 题型:
美国魏考克斯合成的一种有机分子,像一尊释迦牟尼佛。称为释迦牟尼分子。有关该有机分子的说法正确的是 ( )

A.该有机物属于苯的同系物
B.1mol该有机物完全燃烧需消耗25molO2
C.1mol该有机物最多可以和10molH2发生加成反应
D.该有机物的一氯代产物的同分异构体有12种
查看答案和解析>>
科目: 来源: 题型:
我国“神舟五号”载人飞船成功发射,表明我国的载人航天技术已位列于世界前列,在运载飞船的某些火箭推进器中盛有液态肼(N2H4)和液态双氧水,它们充分混合反应后的产物之一是( )
A.氧气 B.氢气 C.氨气 D.氮气
查看答案和解析>>
科目: 来源: 题型:
将一定量的钠、铝金置于水中,合金全部溶解,得到20mL,pH=14的溶液。然后用1mol?L-1的盐酸滴定至沉淀量最大时,消耗盐酸40mL。试通过计算求原合金中钠的质量。
查看答案和解析>>
科目: 来源: 题型:
近年来,我国科学家对有机物的“自由基”的研究有新的突破,在国际上占有领先的地位。有机物中常见的最简单的自由基是碳烯(: CH2),它十分活泼,很容易用它的一对未成对电子与不饱和烃反应,生成三碳环;也可以插在烷基的碳氢键(C―H)之间,使碳链增长。请回答下列问题:
(1)写出碳烯的电子式 。
(2)写出碳烯与丙烯反应产物的结构简式 。
(3)碳烯与烃A反应,生成烃B,一定量的B完全燃烧生成8.8gCO2和4.5gH2O,B分子中含有3个―CH3,且能完成下列转化关系;
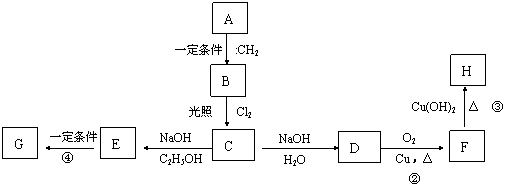
高分子
i写出B结构简式 ;反应①的类型 。
ii 写出反应①的反应方程式 。
iii H的同分异构体有多种,请写出其中能和NaOH反应但不能与NaHCO3反应的H的同分异构体的结构简式(不包括H本身)
; ;
; 。
查看答案和解析>>
科目: 来源: 题型:
在一定条件下发生反应2SO2(g)+O2(g) ![]() 2SO3(g);
2SO3(g);
(1)500℃时,将a molSO2与b molO2以3:2通入固定容积为5L的密闭容器中。
①反应进行至10min时,测得n(SO2)=8mol,n(SO3)=4mol,则b= mol。
②反应进行至10min时,测得反应放热392kJ,则上述热化学方程式中的
△H= kJ/mol。
③10min内平均速率n(SO2)= mol/(L?min)。
④反应达到平衡后,测得容器内压强是反应起始压强的0.715倍,则平衡时
c(SO3)= mol/L,SO2的转化率a1(SO2)= 。
(2)当反应温度、起始SO2与O2物质的量均与(1)相同时,将其混合气通入一恒压反应容器中,达平衡时SO2的转化率a2与(1)SO2的转化率a2的关系是:a2 a1(填=、>或<)
查看答案和解析>>
科目: 来源: 题型:
甲、乙、丙、丁是4种短周期元素,它们的原子序数依次增大,其中甲和丙、乙和丁分别是同主族元素,又知乙、丁两元素的原子核中质子数之和是甲、丙两元素原子核中质子数之和的2倍,甲元素的一种同位素核内无中子。
(1)丙、丁组成的常见化合物,其水溶液呈碱性,原因是(用离子方程式表示) 。写出均含甲、乙、丙、丁四种元素的两种化合物相互间发生反应,且生成气体的离子方程式 。
(2)丁的单质能跟丙的最高价氧化物水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式 。
(3)甲、乙、丁中某两种元素两丙组合可形成A、B两种微粒,它们均为负一价双原子阴离子,且A有18个电子,B有10个电子,则A与B反应的离子方程式为 。
(4)4.0g丁单质在足量的乙单质中完全燃烧,放出37kJ热量,写出其热化学方程式 。
(5)用甲元素的单质与乙元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特制的防止透过的隔膜,在A极通入甲的单质,B极通入乙的单质,则A极是该电池的 极;B极的电极反应式是 。
查看答案和解析>>
科目: 来源: 题型:
下列各物质为中学化学中常见物质,其中A、C、E、F为气体,B、D为无色液体,D是一种重要的化工原料,F的浓溶液与X共热通常用于实验室制备单质,C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。

试回答下列问题:
(1)B的电子式为 。
(2)写出反应②的化学方程式 。
(3)写出反应①、⑥的离子方程式
① ;⑥ 。
(4)根据图中信息,B、C、D、X氧化性从强到弱的顺序是(用对应物质的化学式表示)
。
查看答案和解析>>
科目: 来源: 题型:
(1)已知25℃时几种物质(溶液浓度为0.1mol/L)的电离度如下表:(电离度:弱电解质已电离的分子的物质的量占分子总物质的量的百分数)(已知:H2SO4的第一步电离是完全的)
| ①H2SO4溶液中的HSO | ②NaHSO4溶液中的HSO | ③CH3COOH | ④HCl |
| 10% | 29% | 1.33% | 100% |
i25℃时,0.1mol/L上述几种溶液c(H+)由大到小的顺序是(填序号) .
ii25℃时,将足量的Zn粉放入等体积、pH=1的上述几种溶液中,产生氢气的体积(同温同压下)由大到小的顺序是(填序号) .
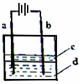 (2)由于Fe(OH)2极易被氧化,所以实验室难以用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用下图所示实验装置,可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
(2)由于Fe(OH)2极易被氧化,所以实验室难以用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用下图所示实验装置,可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
i a电极材料为 ,其电极反应式为 ;
电解过程中,b极附近溶液pH= (增大、减小、不变),
试用必要的文字说明原因 。
ii d电解液是 时,电解片刻后,装置中可见Fe(OH)2白色沉淀。
A.稀硫酸 B.NaCl溶液
C.NaOH溶液 D.CuCl2溶液
iii 装置中液体c的作用是 。
查看答案和解析>>
科目: 来源: 题型:
某学生用邻苯甲酸氢钾( ![]() 相对分子质量为204.0)测定未知的NaOH溶液的浓度,在本实验中到达滴定终点时,溶液的pH约为9.1。
相对分子质量为204.0)测定未知的NaOH溶液的浓度,在本实验中到达滴定终点时,溶液的pH约为9.1。
(1)该学生用托盘天平称量邻苯二甲酸氢钾时(两边均放等质量的纸片),在左盘放一个1g砝码,平衡时游码位置如图所示:
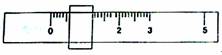
由此可知,所取邻苯二甲酸氢钾的质量为 g.
(2)将称好的邻苯二甲酸氢钾放于锥形瓶中,加适量水溶解,溶液无色,再加入指示剂(从甲基橙、酚酞、石蕊中选择)1~2滴,用NaOH溶液滴定至终点时的现象是
。
(3)该学生进行三次实验,所取固体质量均相同,所需氢氧化钠溶液的体积如下表:
| 实验编号 | NaOH溶液的体积(mL) |
| 1 | 18.2 |
| 2 | 17.1 |
| 3 | 16.9 |
滴定中误差较大的是第 次实验;造成NaOH溶液体积偏大误差的原因不可能有(填序号) 。
①未用氢氧化钠溶液洗涤滴定管②滴定前平视,滴定后俯视 ③滴定前滴定管尖嘴处有气泡,滴定后气泡消失 ④滴定前,锥形瓶用邻苯二甲酸氢钾溶液润洗
(4)NaOH溶液的物质的量浓度为(只列出计算式,不必求出结果) mol/L。
查看答案和解析>>
科目: 来源: 题型:
常温下,将m mL NO2和NO混合气通入过量饱和NaHCO3溶液中,再使逸出的气体通过装有Na2O2(过量)的干燥管,最后收集到n mL b气体,据NO2和NO的体积比推断b的成分,正确的是 ( )
A.当V(NO2):V(NO)=3:1时,b为NO2
B.当V(NO2):V(NO)<3:1时,b为O2
C.当V(NO2):V(NO)>3:1时,b为NO和NO2
D.当V(NO2):V(NO)=3:1时,b为NO2和O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com