
科目: 来源: 题型:
原子经济性是衡量化学反应绿色化的重要指标,原子经济性用原子利用率来衡量,原子利用率等于目标产物质量与产物总质量之比。硫代硫酸钠晶体俗称海波(Na2S2O3?5H2O)或大苏打,它是化学上重要的氧化还原反应的滴定剂,下图是工业上某种制备硫代硫酸钠的流程示意图。已知M为黑色固体纯净物,只含有两种元素,且两种元素质量比为7:4;反应(V)的化学方程式为Na2SO3+S=Na2S2O3。
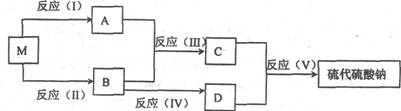
(1)写出反应(I)的离子方程式:______________________________________________。
(2)写出反应(Ⅱ)的化学方程式:_____________________________________________。
(3)反应(V)中,当有1molNa2S2O3生成时,转移的电子总数为_____________________。
(4)反应(I)和反应(II)中投入M的物质的量之比为_____________时,符合绿色化学的要求;理论上,1molM最多能制取Na2S2O3?5H2O的质量为________。
查看答案和解析>>
科目: 来源: 题型:
在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+B2(g)―2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示。
 (1)该反应进行到__________时达到平衡,用AB表示的平均反应速率为:__________(分数表示)。
(1)该反应进行到__________时达到平衡,用AB表示的平均反应速率为:__________(分数表示)。
(2)图中对应的a的数值是_________,该反应的化学平衡常数Kc=__________(保留分数)。温度升高Kc值___________(填“增大”、“减少”或“不变”)。
(3)在上述反应达到平衡后,第4min时,若将容器的体积快速扩大一倍(其他条件不变),请在上图中画出4min~5min的AB浓度的变化线。
(4)在相同条件下,若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol。则反应向__________方向进行(填“正反应”或“逆反应”)。判断依据是______________;反应达到平衡后,各物质的体积分数与原平衡相比___________(填序号)
①A2、B2减小,AB增大 ②A2、B2增大,AB减小 ③均不变 ④无法确定
查看答案和解析>>
科目: 来源: 题型:
某学生设计如下图的方法对A盐进行鉴定
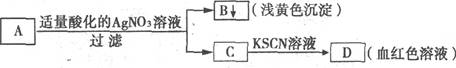
由此分析,下列结论中,正确的是 ( )
A.A中一定有Fe3+ B.C中一定有Fe3+
C.B为AgI沉淀 D.A一定为FeBr2溶液
查看答案和解析>>
科目: 来源: 题型:
常温下经测定某溶液中离子只有Na+、CH3COO-、H+、OH-四种,且离子浓度大小的排列顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。其可能的情形是 ( )
①该溶液由pH=3的CH3COOH、与pH=11的NaOH溶液等体积混合而成 ②0.2mol?L-1的CH3COOH溶液与0.1mol?L-1的NaOH的溶液等体积混合
③该溶液由0.1mol?L-1的CH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合而成
A.① B.② C.①② D.①②③
查看答案和解析>>
科目: 来源: 题型:
我国镍氢电池居世界先进水平,国产大功率镍氢动力电池已广泛用于我海军潜艇。常见镍氢电池的某极是储氢合金LaNi5,电池的总反应为:
LaNi5H6+6NiO(OH) ![]() LaNi5+6Ni(OH)2(LaNi5H6中各元素化合价均为零),下列说法正确的是 ( )
LaNi5+6Ni(OH)2(LaNi5H6中各元素化合价均为零),下列说法正确的是 ( )
A.放电时储氢合金作正极
B. 充电时储氢台金作阴极
C.放电时负极反应:LaNi5H6+6OH-=LiNi5+6H2O+6e-
D.充电时阴极反应:Ni(OH)2+OH--e-=NiO(OH)+H2O
查看答案和解析>>
科目: 来源: 题型:
按下图装置,持续通入X气体,可以看到a处固体变为红棕色,b处变蓝,c处得到液体,则X气体是 ( )
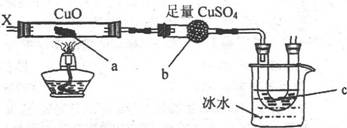
A.H2 B.CO和H2 C.NH3 D.CH3CH2OH(气)
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、R是1~18号元素中的四种元素,它们的原子结构有以下特点:①元素X原子的M层比L层少4个电子;②元素Y的2价阴离子的核外电子排布与氖原子相同;③元素Z原子的L层比M层多5个电子;④元素R原子的L层比K层多1个电子,其中金属性最强的是 ( )
A.X B.Y C.Z D.R
查看答案和解析>>
科目: 来源: 题型:
糖类、脂肪和蛋白质是维持人类生命活动所必需的三大营养物质。以下叙述不正确的是 ( )
A.淀粉水解的最终产物是葡萄糖
B.葡萄糖能发生氧化反应和水解反应
C.植物油能使溴水褪色
D.蛋白质溶液遇硫酸铜后产生的沉淀不能重新溶于水
查看答案和解析>>
科目: 来源: 题型:
碳酸氢铵和熟石灰共热时可能发生如下反应:
NH4HCO3+Ca(OH)2![]() CaCO3+NH3↑+2H2O NH4HCO3
CaCO3+NH3↑+2H2O NH4HCO3![]() NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
取碳酸氢铵和熟石灰的混合物共0.1 mol,在密闭容器中加热至200℃(200℃时CaCO3、Ca(OH)2不分解),充分反应后,排出多余气体,冷却后称量,固体剩余物质量为a g。
(1)若碳酸氢铵和熟石灰以等物质的量混合时,a=_________g。
(2)若以bmol表示混合物中碳酸氢铵的物质的量,通过计算确定a随b变化的数学表达式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com