
科目: 来源: 题型:
金属铝广泛应用于现代生产和日常生活中。
已知:4Al(s)+3O2(g)=2Al2O3(s) △H=-3351.4 kJ?mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) △H=-1633.2 kJ?mol-1
![]() △H=-5518 kJ?mol-1
△H=-5518 kJ?mol-1
将铝用作燃料已成为现实。回答下列问题:
(1)写出工业制铝的阳极电极反应式 。
(2)①铝用作燃料相对于含碳燃料有明显优点,请你写出其中一条 ;
②铝用作燃料相对于氢气也有明显优点,但也有不足,即燃点高。若要在常温常压不使用催化剂的情况下点燃铝,除了应防止表面生成致密的氧化膜外,还应采取的措施是 。
(3)铝热反应在生产中的应用非常广泛。请写出Fe2O3(s)和Al(s)反应的热化学方程式 ;
铝热实验中能看到有熔融物生成,为探究该熔融物的成分,某学生查阅资料如下:
| 物质 | A1 | A12O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | ― |
经分析,该同学推测,铝热反应所得到的熔融物应是铁铝合金。请设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝(简述实验操作、现象及结论) 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
X、Y、Z、R 四种短周期元素,原子序数依次增大。已知:X、R处于同一主族,Y元素的最高正价和最低负价的绝对值相等,X与Y元素形成的一种物质是天然气的主要成分;Y与Z元素形成的一种气体会使大气产生“温室效应”。
请回答下列问题:
(1)X、Y、Z三元素所形成的单质或化合物之间,可按下图装置组成燃料电池。
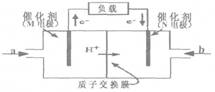
若b口通入的是气体Z2,则a口通入的物质可以是 、 、 (分别填写只由一种、两种、三种元素组成的物质,用化学式表示);M电极的名称为 (填“正极”、“负极”或“阴极”、“阳极”);N电极的电极反应式为 (用化学式表示)。
(2)日常生活中我们经常用到的一种物质其主要成分的化学式为Y18X35Z2R,这种物质的学名为 ,制造这种物质的反应叫 ,写出该反应的化学方程式 。
(3)合成氨工业中,原料气制备的其中一个反应为:YZ+X2Z(g)![]() YZ2+X2;
YZ2+X2;
已知该反应化学平衡常数K和温度T的关系如下表:
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
则下列有关的叙述正确的是 。
A.该反应![]() <0
<0
B.若绝热时(容器内外没有热量交换),改变某一条件平衡向逆反应方向移动,刚容器内气体的温度一定升高
C.若反应在830℃的温度达到平衡状态,反应容器内的四种物质的浓度则一定相等
D.该反应在某温度下,YZ、X2Z的物质的量浓度与时间的关系如下图所示,据此可计算得YZ的转化率为80%

查看答案和解析>>
科目: 来源: 题型:
A、B、C为三种不同短周期非金属元素的单质,化合物E其有漂白性;G分子由形成B、C两单质的两种元素组成,一个G分子中含有18个电子。A→H等物质之间相互转化的关系如下(反应生成的水略去):

(1)若化合物H和F相遇生成固体X时,有白烟产生;则X的溶液中鉴定阳离子的实验方法和现象是
;
(2)反应①的离子方程式为 ;
反应②的化学方程式为 。
(3)若将1 L 0.2mol?L-1的X溶液和1L0.1 mol?L-1的NaOH溶液混合,则得到的溶液中有关离子和分子(H2O除外)的浓度由大到小的关系为 ;
和 两种粒子的物质的量之和比OH-多0.1 mol。
查看答案和解析>>
科目: 来源: 题型:
对室温下pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,有关叙述正确的是( )
A.加入适量的氯化铵晶体后,两溶液的pH均减小
B.温度下降10℃,两溶液的pH均不变
C.分别加水稀释10倍,两溶液的pH仍相等
D.用同浓度的盐酸中和,消耗的盐酸体积相同
查看答案和解析>>
科目: 来源: 题型:
下列实验中金属或氧化物可以完全溶解的是 ( )
A.0.1 mol锌片投入到100 mL 1 mol?L-1的盐酸溶液中
B.1 mol MnO2粉末与400 mL10 mol?L-1的盐酸共热
C.常温下1mol铝片投入到200mL18.4mol?L-1硫酸中
D.常温下 1 mol铜片投入含4molHNO3的浓硝酸中
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,不正确的是 ( )
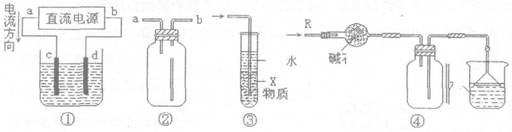
A.装置①中,c为阳极、d为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是 ( )
A.NaHCO3溶液中加入盐酸:CO32-+2H+=CO2↑+H2O
B.紫色石蕊试液中滴入氢硫酸变红的原因是:H2S![]() 2H++S2-
2H++S2-
C.将NaHSO4溶液滴入Ba(OH)2溶液中至pH=7:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
D.电解CuSO4溶液:Cu2++2H2O![]() Cu+O2↑+4H+
Cu+O2↑+4H+
查看答案和解析>>
科目: 来源: 题型:
下图是198 K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是( )

A.该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92 kJ?mol-1
2NH3 △H=-92 kJ?mol-1
B.向一密闭容器中加入1 mol N2和3 mol H2充分反应后,放出92 kJ热量
C.b曲线是加入催化剂时的能量变化曲线
D.加入催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目: 来源: 题型:
具有相同电子层结构的三种微粒An+、Bn-、C,下列分析正确的是( )
A.原子序数关系是C>B>A B.离子半径的关系是Bn-<An+
C.A、B能形成1:1型化合物 D.原子半径的关系是A<C<B
查看答案和解析>>
科目: 来源: 题型:
下列是某学生自己总结的一些规律,其中正确的是( )
A.氧化物不可能是还原产物,只可能是氧化产物
B.有些化学反应不属于化合、分解、置换、复分解中的任何一种反应
C.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
D.将Mg(HCO3)2溶液加热,最终得到Mg(OH)2沉淀,由此可知KSP[Mg(OH)2]>KSP(MgCO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com