
科目: 来源: 题型:
在硫酸的工业制法中,下列生产操作与说明生产操作的原因二者都正确的是 ( )
A.矿石燃烧前需要粉碎,因为大块矿石不能燃烧
B.从沸腾炉出来的炉气需净化,因为炉气中二氧化硫会与杂质反应
C.SO2被氧化为SO3时需使用催化剂,这样可提高SO 2的转化率
D.SO3用98.3%的浓H2SO4吸收 ,能提高吸收效率的防止形成酸雾
查看答案和解析>>
科目: 来源: 题型:
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油
⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.②⑤⑥⑦⑧ D.③④⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
下列关于电解槽的叙述中不正确的是( )
A.电子从源的负极沿导线流入电解槽的阴极
B.与电源负极相连的是电解槽的阴极
C.与电源正极相连的是电解槽的阴极
D.在电解槽的阳极发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
把2.24g铁和100mL稀HNO3溶液混合后充分反应,铁和HNO3均无剩余,向反应后的溶液中加入50mL 0.2mol?L-1的KI溶液,恰好使溶液中的Fe3+全部还原为Fe2+。求原稀HNO3 的物质的量浓度?
查看答案和解析>>
科目: 来源: 题型:
镁、铝、硅的混合物25g,跟足量盐酸反应生成氢气22.4L(标况),另取同样质量的此混合物跟足量烧碱溶液反应,产生氢气仅为前者的一半,试计算原混合物中镁、铝、硅质量各为多少g?
查看答案和解析>>
科目: 来源: 题型:
资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。

(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是________;碱石灰的作用是________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是___________________________________________;
试管内气体变为红棕色,该反应的化学方程式是_____________________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因_______________________________。
(3)将过量的氧气与A产生的氨气分别从A.b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是____,其理由是A. ___B._____________。
②氨气燃烧的化学方程式是______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A~N均为中学化学中的常见物质,其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料,单质M是目前使用量最大的金属,常温下B、E、F为气体,G为无色液体,这些物质在一定条件下存在如下转化关系,其中有些反应物或生成物已经略去。回答下列问题:
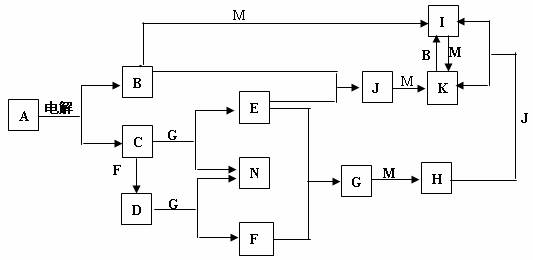
(1)H的化学式为 ,D的电子式为 。
(2)K转变为I的离子方程式: 。
(3)D与G反应的化学方程式为 。
(4)I可用于净水,其原因是
(用相关的反应方程式和简要文字回答)。
(5)1mol气体E在气体F中完全燃烧生成液态G时放出的热量为a kJ,请写出表示E燃烧热的热化学方程式 。
(6)I与NaClO在碱性条件下反应,是制备理想的绿色水处理剂(Na2MO4)的一种方法,试写出此反应的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
饮用水质量是关系人类健康的重要问题。
(1)氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为____________,所生成的次氯酸的电子式为:____________。
(2)写出工业上制取漂白粉的化学反应方程式:____________________________。
(3)ClO2被称为“第四代”饮用水杀虫剂,因其高效率,无污染而被广泛使用.制备ClO2是发达国家普遍重视的课题,我国北京永利科技有限公司已用电解法批量生产ClO2。其反应原理为:4ClO 3―+4H+=4 ClO2+O 2↑+2H 2O 试写出两电极反应式:
阴极:_______________________________________________________
阳极:_______________________________________________________
(4)相同物质的量的氯气与二氧化氯消毒时转移电子数目之比是__________________
(5)采用氧的一种同素异形体用于自来水消毒,既提高了消毒效率,安全无副作用,该物质在自然界中存在,对地球生命体起保护伞作用。该物质和氯气溶于水以及SO2的漂白原理分别是_____________,____________________,__________________;若将氯气与SO2二者混合,若想使石蕊试液褪色则![]() 范围为____________。
范围为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com