
科目: 来源: 题型:
将0.05 mol?L-1的盐酸溶液和未知浓度的氢氧化钠溶液以12的体积比混合,所得混合溶液的c(OH-)=0.01 mol?L-1。用上述氢氧化钠滴定20mL c(H+)=0.001 mol?L-1的某一元弱酸溶液,达到终点消耗12.5mL氢氧化钠溶液.试求:
(1)氢氧化钠溶液的物质的量浓度
(2)此一元弱酸的物质的量浓度
(3)此一元弱酸的电离度
查看答案和解析>>
科目: 来源: 题型:
某温度下在恒容的密闭容器中发生如下反应:2M(g)+N(g) ![]() 2E(g),若开始时只充入2 molE(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2 molM和1 molN的混合气体,达平衡时M的转化率是多少?(要有简单计算过程)
2E(g),若开始时只充入2 molE(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2 molM和1 molN的混合气体,达平衡时M的转化率是多少?(要有简单计算过程)
查看答案和解析>>
科目: 来源: 题型:
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g) + 2 H2(g) ![]() CH3OH(g)不同温度时甲醇的物质的量随时间变化曲线如图所示。根据题意完成下列各题:
CH3OH(g)不同温度时甲醇的物质的量随时间变化曲线如图所示。根据题意完成下列各题:
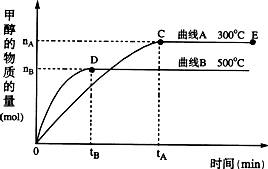
(1)反应达到平衡时,平衡常数表达式k = ,升高温度,k值 (填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,H2的平均反应速率v(H2)= mol?(L?min)-1(用相关符号和数据表示)
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a. 氢气的浓度减小 b. 平衡常数k增大
c. 甲醇的物质的量增加 d. 重新平衡时n(H2)/n(CH3OH)增大
e. 正反应速率加快,逆反应速率也加快
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
将氯化铝溶液蒸干并灼烧得到的固体物质是________,原因是_________________________
____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
现有下列两组溶液(Ⅰ)组:0.1 mol?L-1的醋酸和盐酸,(Ⅱ)组:pH =11的氨水和氢氧化钠溶液。若将它们加水稀释相同的倍数,试比较(Ⅰ)组和(Ⅱ)组溶液pH值的大小:(Ⅰ)组_______ _ ,(Ⅱ)组_________ __。
查看答案和解析>>
科目: 来源: 题型:
请写出醋酸在溶液中的电离方程式__________________________________,
要使0.1mol/L的醋酸溶液中c(H+)/c(CH3COOH)比值增大,可以采取的措施是________________________________(写两种。)
查看答案和解析>>
科目: 来源: 题型:
按要求完成下列反应式
硫化钠水解化学方程式____________________________
碳酸氢钠电离___________________________
碳酸氢钠水解的离子方程式________________________
铅蓄电池反应方程式______________________________
电解氯化钡溶液离子方程式________________________
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,一定量的Ca(OH)2饱和溶液中,加入少量的CaO并维持温度不变,则下列说法中正确的是( )
A.溶液的pH值增大 B.溶液的pH值减小
C.溶液中的Ca2+总数减少 D.溶液中的Ca2+总数增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com