
科目: 来源: 题型:
某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
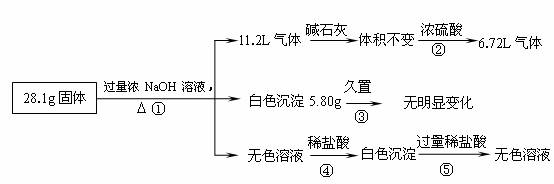
回答下列问题:
(1)混合物中是否存在FeCl2 __ _ (填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4 _ __ (填“是”或“否”),你的判断依据是:
___________________________ 。
(3)写出反应④的离子反应式: 。
(4)请根据计算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程):
查看答案和解析>>
科目: 来源: 题型:
如下图所示的装置,C、D、E、F、X、Y都是惰性电极。
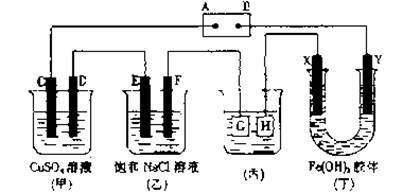
将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答以下问题:
(1)电源A极的名称是___ ____。
(2)甲装置中电解反应的总反应离子方程式是:___________________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是______ ______。
(4)欲用丙装置给铜镀一层银,G应该是_______(填“铜”或“银”),电镀液的主要成分是______ ___(填化学式)。
(5)装置丁中的现象是______________________,说明________ _____ 。
查看答案和解析>>
科目: 来源: 题型:
下列实验操作或对实验事实的叙述正确的是___________(填序号):
①用碱式滴定管量取20.00 mL 0.10mol/L KMnO4溶液;
②用托盘天平称取10.50 g干燥的NaCl固体;
③各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘纸上称量;
④配制Al2(SO4)3溶液时,加入少量的稀硫酸;
⑤将未经湿润的pH试纸浸到某溶液中,过一会取出与标准比色卡比较测得该溶液的pH;
⑥中和滴定中,锥形瓶用蒸馏水洗净后可直接往其中注入一定量的待测溶液;
⑦测定硫酸铜晶体中结晶水含量的实验至少需要加热2次,至少需要称量4次。
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
| A | |||||||||||||||||
| B | C | D | |||||||||||||||
| E | F | ||||||||||||||||
(1)B和E的最高价氧化物对应的水化物中酸性较强的是 (填化学式),写出可以验证该结论的一个离子反应方程式 。
(2)王水可溶解不能与硝酸反应的金属如Au、Pt等,其原因是王水中不仅含有HNO3、还有反应生成的Cl2和NOCl,假设NOCl中所有原子都达到了8电子稳定结构,试写出NOCl的电子式 。
(3)EBC-和A2D2在碱性条件下反应生成了ED42-和可参加大气循环的两种无毒无害气体及水,试写出该反应的离子方程式__________________________。
查看答案和解析>>
科目: 来源: 题型:
用惰性电极电解NaCl与NaHCO3混合溶液,测得溶液pH变化如下图所示。
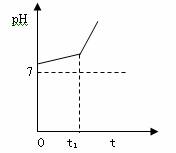
① 在0→t时间内,两个电极上的电极反应式为:
阳极 ;
阴极 。
②用离子方程式表明0→t1时间内,溶液pH升高比较缓慢的原因:
。
查看答案和解析>>
科目: 来源: 题型:
向pH=6的蒸馏水和c(H+)=10-6mol?L-1的稀盐酸中分别投入大小、质量相同的金属钠,反应刚开始时,产生H2的速率前者与后者相比是 (填选项序号)。
A.一样快 B.前者快 C.后者快 D.无法比较
查看答案和解析>>
科目: 来源: 题型:
下图是一水溶液在pH从 0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率[H2CO3]、[HCO3-]、[CO32-],下列叙述正确的是 ( )
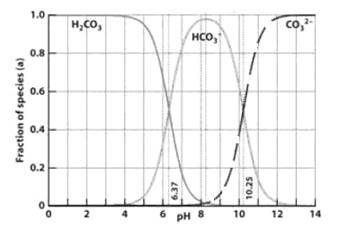
A.此图可完全根据1.0 mol/LHCl溶液滴定1.0mol/L碳酸钠溶液的实验数据绘出
B.1.0 mol/LHCl溶液滴定1.0mol/L碳酸钠溶液恰好反应时呈中性
C.二氧化碳溶解在血液中多以HCO3-的形式存在
D.在pH为6.37及10.25时,溶液中[H2CO3]=[ HCO3-]=[ CO32-]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com