
科目: 来源: 题型:
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
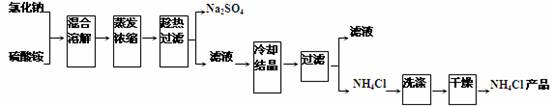
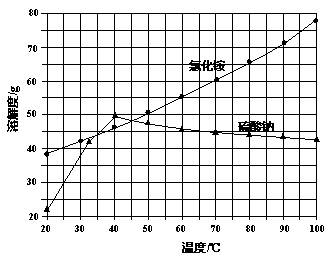
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需 NaCl g。
(2)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为 。
(4)不用其它试剂,检查NH4Cl产品是否纯净的方法及操作是 。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是 。
查看答案和解析>>
科目: 来源: 题型:
将1mol I2(g)和2mol H2(g)置于某2L密闭容器中,在一定温度下发生反应:
I2(g)+H2(g)![]() 2HI(g); ΔH<0,并达到平衡。HI的体积分数Φ(HI)随时间变化如图曲线(II)所示:
2HI(g); ΔH<0,并达到平衡。HI的体积分数Φ(HI)随时间变化如图曲线(II)所示:
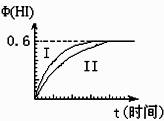
(1)达平衡时,I2(g)的物质的量浓度为 mol?L-1。
(2)若改变反应条件,在某条件下Φ(HI)的变化如曲线
(I)所示,则该条件可能是 (填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),发生反应达平衡时,HI的体积分数仍为0.60,则a、b、c的关系为 (用一个含a、b、c的代数式表示)。
(4)室温时将0.01 mol HI气体溶于水配成100 ml溶液,则该溶液中由水电离产生的氢离子的物质的量浓度为 mol?L-1 ;若降低温度该溶液的pH值将 (填增大、减小或不变)
查看答案和解析>>
科目: 来源: 题型:
A、B、C是中学化学中常见的无机物,且各由两种元素组成;甲、乙、丙是三种常见的单质;这些化合物和单质间存在如下图所示转化关系(这些转化关系都不需要使用催化剂)。
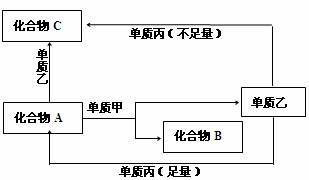
请回答下列问题:
(1)若甲在转化中为还原剂,是常见金属,乙是常见非金属单质,丙可以使带火星的木条复燃,且甲、乙、丙由短周期元素组成。则A的结构式是 ,A与甲反应的化学方程式是 。
(2)若甲在转化中为氧化剂,是常见非金属气态单质,丙是常见金属,甲、乙、丙中只有甲由短周期元素组成,且乙与甲同主族,与丙同周期,乙是常温下唯一的液体非金属单质,也有强氧化性。通常条件下反应都在溶液中进行。则:
①单质丙是(写元素符号) 。
②A与乙反应的离子方程式为 。
③当A与甲的物质的量之比为2:3时,A与甲恰好完全反应,并符合上图所示,则A的溶液跟甲反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:先配制100mL 0.10 mol?L-1 NaOH标准溶液,然后取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作3次,记录数据如下。
| 实验编号 | NaOH溶液的浓度 (mol?L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.02 | 20.00 |
| 2 | 0.10 | 21.92 | 20.00 |
| 3 | 0.10 | 22.06 | 20.00 |
①滴定达到终点的标志是___________________________________________
②根据上述数据,可计算出该盐酸的浓度_______________
③排去碱式滴定管中气泡的方法应采用操作_________________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

甲 乙 丙
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_____(多选扣分)
A.滴定终点读数时俯视读数
B.碱式滴定管尖嘴部分有气泡,滴定后消失
C.锥形瓶水洗后未干燥
D.锥形瓶水洗后用待测稀盐酸溶液润洗
E.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
查看答案和解析>>
科目: 来源: 题型:
指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):___________________________________________。
②容量瓶:________________________________________________________。
③托盘天平________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被80mL浓度为0.5 mol?L-1的HCl溶液中和,则生成物的成分是 ( )
A.Na2O B.Na2O2 C.Na2O2和NaO2 D.Na2O和Na2O2
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是( )
A.中子数决定元素的不同核素
B.半径顺序: Cl->S2->Ca2+>K+
C.短周期元素形成的阴阳离子电子数之差可能为:0、6、8、18
D.离子化合物中不含共价键
查看答案和解析>>
科目: 来源: 题型:
有 ① Na2CO3溶液 ② CH3COONa溶液 ③ NaOH溶液各25mL,物质的量浓度均为
0.1 mol?L-1,下列说法正确的是( )
A.3种溶液pH的大小顺序是 ③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25 mL 0.1 mol?L-1盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
查看答案和解析>>
科目: 来源: 题型:
下列各组物质,用一种试剂无法区别的是( )
A.三种浓酸:HNO3、H2SO4、HCl
B.四种黑色粉末:MnO2、FeO、Fe、CuO、C
C.四种白色粉末:(NH4)2SO4、NH4Cl、Na2SO4、NaCl
D.四种无色溶液:NaCl、NaOH、KOH、KCl
查看答案和解析>>
科目: 来源: 题型:
下列各溶液中,微粒的物质的量浓度关系不正确的是 ( )
A.1.0 mol?L-1 Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.1.0 mol?L-1NH4Cl溶液:c(NH4+)<c(Cl-)
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com