
科目: 来源: 题型:
已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8mol?L-1,AgCl的饱和溶液中c(Ag+)为1.30×10-5mol?L-1。若在5mL含有KCl和KI浓度均为0.01mol?L-1的混合溶液中,滴加8mL 0.01mol?L-1的AgNO3溶液,则下列叙述中不正确的是( )
A.溶液中所含溶质的离子浓度大小关系为:c(K+)>c(NO―3)>c(Ag+)>c(Cl-)>c(I-)
B.溶液中先产生的是AgI沉淀
C.AgCl的KSP的数值为1.69×10-10
D.若在AgI县浊液中滴加少量的KCl溶液,黄色沉淀不会转变成白色沉淀
查看答案和解析>>
科目: 来源: 题型:
下列实验操作或实验事故的处理正确的是( )
A.做焰色反应时,用玻璃棒蘸取溶液放在酒精灯上灼烧
B.分液时,下层液体先从下口放出,换一个接受容器,再将上层液体从下口放出
C.浓NaOH溶液粘到皮肤上,先用稀硫酸冲洗,再用水冲洗
D.稀释浓硫酸时将浓硫酸沿烧杯壁慢慢注入水中并不断搅拌
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是1.0×10-amol?L-1和1.0×10-bmol?L-1,在此温度下,则下列说法正确的是( )
A.a<b
B.a=b
C.水的离子积为1.0×10-(7+a)
D.水的离子积为1.0×10-(b+a)
查看答案和解析>>
科目: 来源: 题型:
下列化学反应的离子方程式正确的是( )
A.碳酸氢钙溶液中加入氢氧化钠溶液:HCO―3+OH―== CO2―3+H2O
B.金属铝溶于氢氧化钠溶液:2Al+6OH―==2AlO―2+3H2↑
C.用FeCl3溶液腐蚀铜电路板:2Fe3++Cu == 2Fe2++Cu2+
D.以石墨作电极电解氯化铝溶液:2Cl―+2H2O![]() 2OH―+H2↑+Cl2↑
2OH―+H2↑+Cl2↑
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物
B.蒸馏和蒸发分别可以从海水中得到淡水和粗盐
C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质
D.电解质溶液导电过程是物理变化
查看答案和解析>>
科目: 来源: 题型:
节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务。下列举措不符合这一要求的是( )

A.将煤液化、气化,提高燃料的燃烧效率
B.为保证饮食卫生大力提倡使用一次性筷子
C.进一步推广使用乙醇汽油作为汽车的燃料
D.洗涤衣物时合理使用无磷洗衣粉等洗涤剂
查看答案和解析>>
科目: 来源: 题型:
下列框图中A、F、G、H都是芳香族化合物。A的相对分子质量不超过200,完全燃烧只生成CO2和H2O;A中氧元素的质量分数为![]() 。
。
又已知:①G、E均能发生银镜反应;②F与NaHCO3溶液反应能产生气体。③C的溶液被称为福尔马林。

回答下列问题:
(1)E产生的核磁共振氢谱图上有 种峰。
(2)C和苯酚反应生成酚醛树脂的反应类型为(选填序号) 。
①消去反应 ②取代反应 ③加成反应 ④缩聚反应
(3)一个A的分子中应有 个(选填2、3、4……等)氧原子。
(4)由F生成H的化学方程式为 。
(5)H的同分异构体甚多。请写出符合下列条件的同分异构体的结构简式(任写两种):
①苯环上只有一个取代基;②能够与NaOH溶液反应。
。
查看答案和解析>>
科目: 来源: 题型:
下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。
(1)请写出下图中d单质对应元素原子的电子排布式 。

(2)单质a、f对应的元素以原子个数比1:1形成的分子(相同条件下对H2的相对密度为13)中含 个![]() 键和 个
键和 个![]() 键。
键。
(3)a与b的元素形成的10电子中性分子X的空间构型为 ;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到配合物的化学式为 ,其中X与Ag+之间以 键结合。
(4)下图是上述六种元素中的一种元素形成的含氧酸的结构:请简要说明该物质易溶于水的原因 。

查看答案和解析>>
科目: 来源: 题型:阅读理解
某校甲、乙、丙三个化学兴趣小组利用课外活动时间,设计了不同的课题分别进行了实验探究活动:
(1)甲小组进行中和滴定实验,实验室里只提供了下面几种仪器:酸式滴定管、碱式滴定管、量筒、托盘天平、普通漏斗、玻璃棒、烧杯,你认为还缺少的玻璃仪器是 。
(2)乙小组设计了如图所示的一套实验装置,以探究该装置的多功能性。
①李明同学认为该装置可以用来制取、收集SO2气体,其中III中盛有NaOH溶液。乙小组同学经过讲座后认为该装置存在安全隐患,需要将III进行改装,请将改装后的装置图画在方框内。
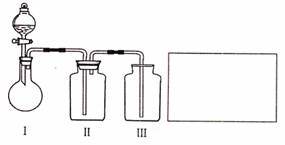
②王强同学认为可利用该装置快速制取、净化、收集氨气,其中II中盛有浓H2SO4。你认为是否正确,若正确则不需做答;若不正确,提出改进意见: 。
(3)丙小组进入了一家回收含铜电缆废料的工厂做社会调查,技术员向同学们展示了两个处理方案,并向同学们提出了下列问题:
方案1:
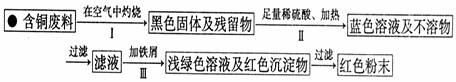
方案2:

①你认为方案 更符合当前绿色生产理念。
②写出方案1中步骤Ⅱ反应的离子方程式 。
③技术员指出,无论是方案1还是方案2,都应加入稍过量的铁屑并最终除去,请你设计除去铁屑的操作方法 。
④为了增加经济效益,该工厂把最后一步所得浅绿色溶液,通过 、冷却结晶、过滤、洗涤、自然干燥得到一种俗称“绿矾”的工业产品。
⑤丙组同学经查询资料,研究、讨论,又设计了方案3,即把方案2中“加入足量稀硫酸、通入空气并加热”改为“加入足量稀硫酸和H2O2”,也可以得到同样的结果。该反应的化学方程式是 。
查看答案和解析>>
科目: 来源: 题型:
下图每一方框中的字母代表一种反应物或生成物。

(1)若X由M、N两种短周期且同周期元素形成 ,M原子的最外层电子数是最内层电子数的![]() N元素最高正价与它的负价代数和为6。
N元素最高正价与它的负价代数和为6。
①写出反应Ⅱ的离子方程式 。
②下图为IV达到平衡后改变反应条件,反应速率随时间变化的情况,已知t2-t3阶段为便用催化剂;t3-t4阶段为减小体系的压强,写出符合上述条件的化学方程式 (写一个即可,用具体物质表示);若t4-t5阶段为升高体系的温度,则该反应为 (填“放热”或“吸热”)
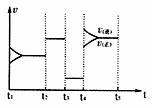
③某温度下,四个容器中均进行着上述反应,各物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器编号 | C(C)/mol?L―1 | C(D)/mol?L―1 | C(G)/mol?L―1 | V正、V逆比较 |
| 甲 | 0.06 | 0.60 | 0.60 | V正=V逆 |
| 乙 | 0.6 | 0.50 | 0.40 | |
| 丙 | 0.12 | 0.40 | 0.80 | V正<V逆 |
| 丁 | 0.12 | 0.30 | V正=V逆 |
(2)若X是一种含氧酸盐,B是金属单质,C、D是非金属单质,反应Ⅱ需要B与A的浓溶液共热才能进行,且生成的E与G是同一种物质。写出反应Ⅰ的化学方程式 ;4g固态D在C中完全反应放出37.2kJ的热量,写出该反应的热化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com