
科目: 来源: 题型:
将20mL 0.4mol/L硝酸铵溶液跟50mL 0.1mol/L氢氧化钡溶液混合,则混合溶液中粒子浓度间的关系正确的是( )
A.c(NO![]() )>c(OH―)>c(NH
)>c(OH―)>c(NH![]() )>c(Ba2+)
)>c(Ba2+)
B.c(NO![]() )> c(Ba2+)>c(NH
)> c(Ba2+)>c(NH![]() )>c(OH―)
)>c(OH―)
C.c(NO![]() )= c(NH
)= c(NH![]() )+c(NH3?H2O)+c(NH3)
)+c(NH3?H2O)+c(NH3)
D.2c(Ba2+)+c(H+)= c(NO![]() )+ c(OH―)
)+ c(OH―)
查看答案和解析>>
科目: 来源: 题型:
一定条件下,体积为10L的密闭容器,装入1molX和4molY进行如下反应:
X(g)+3Y(g)![]() 2Z(g);△H<0经过60s达到平衡,生成0.3molZ。下列说法正确的是( )
2Z(g);△H<0经过60s达到平衡,生成0.3molZ。下列说法正确的是( )
A.升高温度或减小压强有利于反应向正方向进行
B.60s内X的平均反应速率为0.00025mol/(L?s)
C.达平衡时物质X与Y的转化率相等
D.其他条件不变,将容器体积扩大为20L,Z的平衡浓度变为原来的![]()
查看答案和解析>>
科目: 来源: 题型:
下列方程式书写正确的是 ( )
A.次氯酸的电离方程式:HClO=H++ClO―
B.铝溶于烧碱溶液的离子方程式:Al+2OH―=AlO![]() +H2↑
+H2↑
C.电解精炼铜的阴极反应式:Cu-2e―=Cu2+
D.稀硝酸与过量铁屑反应的离子方程式:3Fe+8H++2NO![]() =3Fe2++2NO↑+4H2O
=3Fe2++2NO↑+4H2O
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.相同条件下,N2和O2的混合气体与等体积的N2所含的分子数相等
B.18gD2O中含有的质子的物质的量为10mol
C.常温常压下30gNO与22.4LCO所含分子数相等
D.标准状况下,33.6L H2O含有9.03×1023个H2O分子
查看答案和解析>>
科目: 来源: 题型:
下列做法正确的是( )
A.做氢气还原氧化铜的实验,先加热氧化铜再通氢气
B.做分解氯酸钾制取氧气的实验后,把剩余的残渣倒入垃圾桶
C.不慎将少量浓硫酸沾到皮肤上,立刻用在凉水冲洗
D.配制浓硫酸与酒精的混合液时,把酒精加入盛有浓硫酸的烧杯中
查看答案和解析>>
科目: 来源: 题型:
下列各组溶液,不用其它试剂就可以将它们区别开的是( )
A.盐酸、氯化钾、硫酸钾、碳酸钾
B.氢氧化钾、碳酸钾、硫酸镁、硫酸氢钾
C.氯化钡、硝酸钡、硫酸钠、硝酸钾
D.硝酸钠、盐酸、氯化铵、氢氧化钾
查看答案和解析>>
科目: 来源: 题型:
我国已经决定未来15年大力发展太阳能、风能等新能源。从而减少化合能源的使用。此决策的实施有助于控制 ( )
①温室效应 ②二氧化硫排放 ③白色污染 ④臭氧空洞
A.①② B.①②③ C.①②④ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
由KClO3和Al粉组成的混合物甲,与一定量CuO混合均匀,在强热条件下发生如下反应:
2KClO3 2KCl+3O2↑,4Al+3O2 2Al2O3,3CuO+2Al 3Cu+Al2O3反应完全后得到混合物乙。
①向混合物乙中加入稀盐酸至固体不再溶解,恰好用去200mL 3mol/L盐酸,反应中无气体产生,结果得到无色溶液丙和不溶物丁,然后过滤。
②将溶液丙加热,蒸干并灼烧得到固体戊,且戊的质量和甲的质量恰好相等。
回答下列问题:
(1)写出不溶物丁的化学式 ;
写出①中反应的离子方程式: ;
(2)甲中铝粉的质量为 g,KClO3的物质的量为 mol;
(3)溶液丙中所有离子浓度由大到小顺序为 。
查看答案和解析>>
科目: 来源: 题型:
工业制纯碱的第一点是通过饱和食盐水、氨和二氧化碳之间的反应,制取碳酸氢钠晶体。该反应原理可以用以下化学方程式表示,此反应是放热反应。
NH3+CO2+H2O+NaCl(饱和)=== NaHCO3(晶体)↓+NH4Cl
(1)某校学生实验小组利用上述反应原理,设计如图1所示装置,制取碳酸氢钠晶可选用的药品有: a.石灰石b.生石灰c.6mol/L盐酸d.稀硫酸e.浓氨水f.饱和氯化钠溶液。
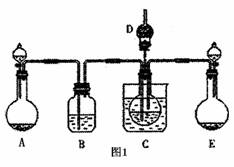
①A中制备气体时,所需药品是(选填字母代号) ;
②B中盛有饱和碳酸氢钠溶液,其作用是 ;
③在实验过程中,向C中通入气体是有先后顺序的,应先通入气体的化学式为
④检验D出口处是否有氨气逸出的方法是 。
(2)该小组同学为了测定C中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图2所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是(选填字母序号)
;
A.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
B.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
C.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②操作Ⅲ的方法为 、 、 ;
③所得晶体中碳酸氢钠的纯度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com