
科目: 来源: 题型:
某同学利用铁与水蒸气反应后的固体物质进行了如下实验:

(1)固体溶于稀盐酸的化学方程式为 。
(2)试剂1的化学式是 。
(3)加入新制氯水后溶液红色加深的原因是(用离子方程式表示):
(4)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设:
假设1:溶液中的+3价铁被氧化为更高的价态;
假设2: ;
②设计方案:
为了对你所提出的假设2进行验证,你设计的实验方案是 。
查看答案和解析>>
科目: 来源: 题型:
已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一氧化还原反应的体系中,共有KCl、Cl2、浓H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(1)该氧化还原反应的体系中,还原剂是______,化合价没有发生变化的反应物是___ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平):
________________________________________________________。
(3)上述反应中,1 mol氧化剂在反应中转移的电子为_______ mol。
(4)如果在反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3-反应后变为无色的
Bi3+。证明NaBiO3的一个性质是:_______________________________________。
查看答案和解析>>
科目: 来源: 题型:
N2在化工生产、农业、医疗、航天航空等诸多领域用途广泛。某化学兴趣小组同学为探究在实验室制备较为纯净N2的方法,进行了认真的准备。请你参与交流与讨论。
[查阅资料] N2的制法有下列三种方案:
方案1:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉。
方案2:加热NaNO2和NH4Cl的浓溶液制得N2。
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2。
[实验准备] 以实验室常见仪器(药品)等设计的部分装置如下图(有的夹持和加热仪器未画出)。
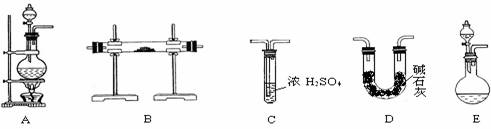
[分析交流]
(1)若按方案1制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的顺序连接的顺序是(填写序号,下同)________ 。
获得N2的反应原理是(写反应方程式)_________________________________。
(2)若以排水法收集N2,其中会混入水蒸气。但也不宜用排空气法,其原因是______
_______________。你提出的收集方法是__________________。
(3)若以方案2制得N2,应选择的发生装置是__________。为保证实验安全顺利进行,操作时应____________________________________________________(填写两点)。
(4)上述三个方案中,制得的N2纯度最差的是__________。在N2纯度要求不甚严格的情况下,有人建议将方案1和方案3结合使用,你认为其优点是______________ 。
查看答案和解析>>
科目: 来源: 题型:
现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、NO3-的相互分离。相应的实验过程可用下列流程图表示:

(1)写出上述实验过程中所用试剂的名称:
试剂1___________试剂2_____________试剂4________________
(2)恰当地控制试剂4的加入量的方法是_________________________________
(3)加入过量试剂3的目的是_______________________________
(4)在加入试剂4后,获得固体D的实验操作④是_______________(填操作名称)
查看答案和解析>>
科目: 来源: 题型:
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 碳酸钠溶液可用于治疗胃病 | Na2CO3可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
| B | 向Na2O2的水溶液中滴入酚酞变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,无 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
| D | 过氧化钠可用于航天员的供氧 | Na2O2能和CO2和H2O反应生成O2 | Ⅰ对,Ⅱ对,有 |
查看答案和解析>>
科目: 来源: 题型:
下列实验中,溶液颜色有明显变化的是( )
A.少量明矾溶液加入到过量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固体加入到过量NaHSO3溶液中
D.往酸性高锰酸钾溶液中滴入足量FeSO4浓溶液
查看答案和解析>>
科目: 来源: 题型:
用下面的方案进行某些离子的检验,其中方案设计得最严密的是 ( )
A.检验试液中的SO![]() :试液
:试液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
B.检验试液中的SO![]() :试液
:试液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
C.检验试液中的![]() :试液
:试液 ![]() 棕黄色溶液
棕黄色溶液 ![]() 蓝色溶液
蓝色溶液
D.检验试液中的CO![]() :试液
:试液![]() 白色沉淀
白色沉淀![]() 沉淀溶解
沉淀溶解
查看答案和解析>>
科目: 来源: 题型:
2008年北京奥运会主体育场――“鸟巢”,被《泰晤士报》评为全球 “最强悍”工程。 “鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓高亮度LED材料。有关说法正确的是( )

A.合金的熔点通常比组分金属高,硬度比组分金属小
B.已知Ga处于ⅢA主族,可推知氮化镓化学式为GaN
C.用金属铝与V2O5冶炼钒,铝作还原剂
D.ETFE膜(![]() )是新型无机高分子材料
)是新型无机高分子材料
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z三种元素的原子序数都不超过20,若:X+与Y-两种离子具有相同的电子层结构;Z元素的核内质子数比Y元素核内质子数少9个,Y和Z两元素可形成42个电子的YZ3―离子。下列说法正确的是 ( )
A.离子半径X+>Y-
B.原子序数X>Y>Z
C.X、Y、Z均属于短周期元素
D.X、Y、Z可形成XYZ、XYZ3、XYZ4等化合物
查看答案和解析>>
科目: 来源: 题型:
某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是 ( )
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I-
A.①③ B.①②③ C.③④ D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com