
科目: 来源: 题型:
下列说法中,不正确的是
A.![]() 与
与![]() 所含中子数相等
所含中子数相等
B.等物质的量的甲基(-![]() )与羟基(-
)与羟基(-![]() )所含质子数相等
)所含质子数相等
C.等物质的量的![]() 与
与![]() 所含电子数与质子数均相等
所含电子数与质子数均相等
D.标准状况下,以任意比例混合的![]() 和
和![]() 混合物22.4L,含有的分子数为
混合物22.4L,含有的分子数为![]()
![]()
查看答案和解析>>
科目: 来源: 题型:
下列除去杂质的方法正确的是
①除去乙烷少量的乙烯:光照条件下通入![]() ,气液分离
,气液分离
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏
③除去![]() 中少量的
中少量的![]() :气体通过盛饱和碳酸钠溶液的洗气瓶
:气体通过盛饱和碳酸钠溶液的洗气瓶
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
A.①② B.③④ C.②④ D.②③
查看答案和解析>>
科目: 来源: 题型:
生活是化学的源泉,下列有关生活中的化学叙述不正确的是
A.铁强化酱油可通过膳食补充人体所需的铁元素
B.不可用铝制餐具长时间存放酸性、碱性食物
C.一定浓度的双氧水可用于伤口的消毒
D.凡含有食品添加剂的食物对人体健康均有害,不宜食用
查看答案和解析>>
科目: 来源: 题型:
某有机物X(C12H12O6Br)遇到FeCl3溶液显紫色,其部分结构简式如下:
已知X在足量的氢氧化钠水溶液中加热,可以得到A、B、C三种有机物。
![]() ① C的核磁共振氢谱只有一个吸收峰
① C的核磁共振氢谱只有一个吸收峰
② 室温下A经盐酸酸化可以得到苹果酸E,E的结构简式为
试回答:
(1)B中所含官能团的名称是 。
(2)C的结构简式为 。
(3)E不能发生的反应类型是 。(填序号)
a.加成反应 b.消去反应 c.氧化反应 d.酯化反应
(4)E的一种同分异构体F有如下特点:1 mol F可以和3mol金属钠发生反应,放出
33.6L H2(标准状况下),1 mol F可以和足量NaHCO3溶液反应,生成1 mol CO2,
1 mol F还可以发生银镜反应,生成2 mol Ag。试写出F可能的一种结构简式:
。
(5)在一定条件下两分子E可以反应生成六元环酯,写出此反应的化学方程式:
。
查看答案和解析>>
科目: 来源: 题型:
(1)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和
食品安全也越来越为人们所关注。甲醛是室内主要空气污染物之一(其沸点是―19.5
℃),甲醇是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高
于甲醛的主要原因是 ;甲醛分子中C的杂化方式为 ,分
子中共有 个π键。
(2)砷化镓属于第三代半导体,它能直接将电能转化为光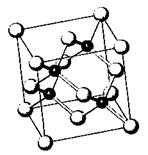 能。已知砷化镓的晶胞结构如
能。已知砷化镓的晶胞结构如
右图。是回答下列问题:
① 下列说法正确的是 (选填序号)
A.砷化镓晶胞结构与NaCl相同
B.第一电离能:As>Ga
C.电负性:As>Ga
D.砷和镓都属于p区元素
② Ga的核外电子排布式为 ;
③ 砷化镓是将(CH3) 3Ga和AsH3用MOCVD方法制备得到,该反应在700℃进行,
反应的方程式为 ;(CH3) 3Ga中碳镓键之间键角为 。
查看答案和解析>>
科目: 来源: 题型:
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最
近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,
MnFe2O4的制备流程如下:

(1)投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为___________。
(2)步骤二中“连续搅拌”的目的是__________________________;
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4![]() MnFe2O4-x+
MnFe2O4-x+![]() O2↑
O2↑
MnFe2O4-x+xH2O→MnFe2O4+xH2↑
请认真分析上述两个反应并回答下列问题:
① 从理论上讲,该循环中,1 mol H2O能制 mol H2
② 若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为______。
③ 针对MnFe2O4热化学循环制氢过程存在的不足,你认为热化学循环制氢还需要
解决的化学问题是 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
某化学课外活动小组在实验室做了如下一系列实验:
(1)该小组设计了如图所示的一套气体发生、收集和尾气吸收装置以探究装置的多功能
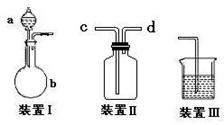 性。
性。
① 甲同学认为装置Ⅰ可作为实验室制氧气的快速发生器,则装置Ⅰ的a仪器中可加
入 或 ,装置Ⅱ从 管口进气即可作为O2的收集装置。
 ② 乙同学认为利用装置Ⅱ,可收集NO,试简述操作方法:
② 乙同学认为利用装置Ⅱ,可收集NO,试简述操作方法:
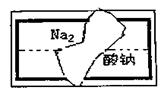
(2)小组在整理实验室的化学试剂时,发现一盛有
无色溶液的试剂瓶。标签破损(如图),请你根
据已掌握的知识,对该试剂可能是什么物质的溶
液作出二种猜想,并设计实验验证,写出任一种
的实验操作、现象和结论。
| 猜想物质的化学式 | 检验所需要的试剂 | 操作、现象和结论 | |
| ① | |||
| ② |
|
(3)该小组从ZnSO4、FeCl3的混合溶液中制取ZnSO4?7H2O过程如下:
a.在混合液中加入6 mol?L―1NaOH溶液,至pH=8为止。
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀。
c.向洗涤后的沉淀中加入2 mol?L―1的硫酸,保持溶液的pH在4~6,加热煮沸,
趁热过滤,滤液即为ZnSO4溶液
d.滤液中注入2 mol?L―1的硫酸,使其pH保持为2……
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列
问题:
| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
① 步骤a中用pH试纸控制溶液pH=8,使用pH试纸的操作是 ;步骤b中如何
检验沉淀已经洗涤干净? 。
② 要制得ZnSO4?7H2O的步骤d还缺少的操作是 ,所用的主要硅酸盐
仪器是 。
查看答案和解析>>
科目: 来源: 题型:
氮是地球上含有丰富的一种元素,氮及其化合物在公农业生产、生活中有着重
要作用,减少N的氧化物在大气中的排放是环境保护的重要内容之一。

(1)上图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,请写出
NO2和CO反应的热化学方程式: ;
又知:N2 (g)+2NO2 (g)=4NO(g) △H=+292.3kJ?mol―1,则反应:
2NO(g)+2CO(g) ![]() N2(g)+2CO2 (g)的△H为 ;
N2(g)+2CO2 (g)的△H为 ;
(2)一定温度下,在2L密闭容器中NO2和O2可发生下列反应:
4NO2 (g)+O2 (g) ![]() 2N2O5(g);已知体系中n(NO2)随时间变化如下表:
2N2O5(g);已知体系中n(NO2)随时间变化如下表:
t(s) | 0 | 500 | 1000 | 1500 |
n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
① 写出该反应的平衡常数表达式:K= ,已知:![]() ,则该反
,则该反
应是 热反应;
② 反应达到平衡后,NO2的转化率为 ,此时若再通入一定量氮气,则NO2
的转化率将 (填“增大”、“减小”、“不变”);
③ 下图中表示N2O5的浓度的变化曲线是 ,
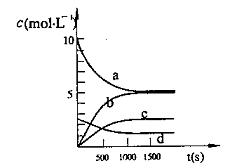
用O2表示从0~500s内该反应的平均速率v= 。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),
其中反应①是置换反应,B、C、F都是气态单质,且B为黄绿色;反应③中有水生成,
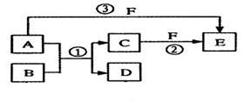 反应②需要放电才能发生,A和D相遇有白烟生成。
反应②需要放电才能发生,A和D相遇有白烟生成。
(1)反应③的化学方程式为: ;
(2)反应①中每生成1 molC,转移的电子数为 ;
(3)A与D的水溶液恰好完全反应时,其生成物的水溶液呈 性(填“酸”“碱”
或“中”),该水溶液中存在着如下关系,用粒子浓度符号填写。
① c(H+)+ = c(OH―)+ ;② c(H+)= c(OH―)+ ;
(4)元素X与组成B的元素同周期,X的单质既可与酸反应也可与碱反应且都生成H2,
则
① X的单质与碱反应的离子方程式 ;
② X、空气、海水可以组成新型海水标志灯的电池。该电池以海水为电解质溶液,
靠 的氧气使X不断氧化而源源不断产生电流,只要把灯放入海水中,数分钟后就
会发出耀眼的闪光,其能量比干电池高20~50倍。则该新型电池的正极的电极反应
式为 ;原电池的总反应方程式为 。
查看答案和解析>>
科目: 来源: 题型:
常温下,0.1mol?L―1某一元酸(HA)溶液中![]() =1×108,下列叙述正确的是( )
=1×108,下列叙述正确的是( )
A.该一元酸溶液的pH=1
B.该溶液中由水电离出的c(H+)=1×10-11mol?L―1
C.该溶液中水的离子积常数为1×10-22
D.用pH=11的NaOH溶液V1L与V2L0.1 mol?L―1该一元酸(HA)溶液混合,若混合
溶液的pH=7,则V1<V2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com