
科目: 来源: 题型:
在120 ℃ 时,以任意质量比混合的某烃的混合物和过量 O2 在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是
A. CH4和C2H4 B. CH4和C2H6 C. C2H4和C2H6 D. C2H2和C3H6
查看答案和解析>>
科目: 来源: 题型:
将等体积的甲烷与氯气混合于一集气瓶中,加盖后置于光亮处,下列有关此实验的现象和结论叙述不正确的是
A.瓶中气体的黄绿色逐渐变浅 B.瓶内壁有油状液滴形成
C.若日光直射,可能发生爆炸 D.生成物只有一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷
查看答案和解析>>
科目: 来源: 题型:
在下图所示的转化关系中。A是一种链状羧酸,分子式为![]() ;F中含有七个原子构成的环;H是一种高分子化合物。请填写下列空白:
;F中含有七个原子构成的环;H是一种高分子化合物。请填写下列空白:
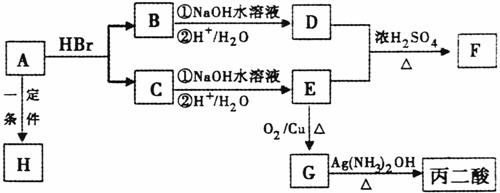
(1)写出F的结构简式:___________
(2)请写出:
①A→H的化学方程式:______________________________________________
②B与![]() 溶液反应的化学方程式:________________________________
溶液反应的化学方程式:________________________________
(3)反应G→丙二酸的反应类型是:______________________________________
查看答案和解析>>
科目: 来源: 题型:
现有部分前四周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| A | 第三周期中的半导体材料 |
| B | L层s电子数比p电子数少1 |
| C | 第三周期主族元素中其第一电离能最大 |
| D | 前四周期呀中其未成对电子数最多 |
(1)B单质分子中,含有________个![]() 键和__________个
键和__________个![]() 键,元素B的气态氢化物的空间型为________________。
键,元素B的气态氢化物的空间型为________________。
(2)C单质的熔点____________A单质的熔点(填“高于”或“低于”),其原因是:_______________
(3)写出元素D基态原子的电子排布式:______________________。
查看答案和解析>>
科目: 来源: 题型:
(12分)某校化学研究小组的同学已知碳酸钠和碳酸氢钠的化学性质,并对碳酸钠和碳酸氢娜的活泼性进行了如下实验探究:
I、为了鉴别碳酸钠和碳酸氢钠两种白色固体,小组成员用不同的方法进行了实验,如下图装置所示:
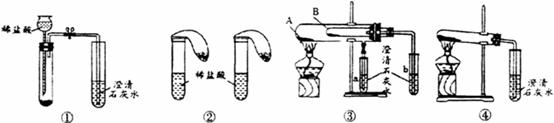
(1)只根据图①、图②所示实验,能够明确达到实验目的的是_______(填“①”或 “②”)
(2)若用图③所示实验装置验证碳酸钠比碳酸氢钠的稳定性好,则碳酸氢钠应装入_________管中(填“A”或“B”)。
(3)有同学提出用图④所示实验装置就能在一次实验、一个反应中比较出碳酸钠和碳酸氢钠的热稳定性相对强弱,你认为这个说法___________(填“正确”或“不正确”)
Ⅱ、已知:10℃时,在烧杯中加入![]() 的
的![]() 溶液400mL,测得该溶液在不同温度下的pH(见下表):
溶液400mL,测得该溶液在不同温度下的pH(见下表):
| 温度(℃) | 10 | 20 | 30 | 50 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 |
甲同学将![]() 的
的![]() 溶液置于烧杯中加热至50℃,测其pH为8.9;再将溶液冷却至20℃,测其pH仍为8.4。乙同学将200mL、20℃、
溶液置于烧杯中加热至50℃,测其pH为8.9;再将溶液冷却至20℃,测其pH仍为8.4。乙同学将200mL、20℃、
![]() 的
的![]() 溶液置于烧杯中加热至90℃一段时间后,将溶液冷却至
溶液置于烧杯中加热至90℃一段时间后,将溶液冷却至
20℃,测其pH为10.1(溶液体积不变)。
请对上述实验现象作出说明。
查看答案和解析>>
科目: 来源: 题型:
(14分)一定条件下铁可以和![]() 发生反应:
发生反应:![]() ,已知该反应的平衡常数(
,已知该反应的平衡常数(![]() )与温度(
)与温度(![]() )的关系如图甲所示:
)的关系如图甲所示:
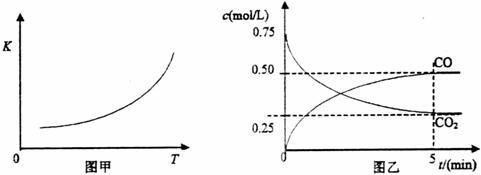
(1)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的![]() 气体,反应过程中
气体,反应过程中
![]() 气体和
气体和![]() 气体的浓度与时间的关系如图乙所示。5min内,CO的平均反应速率
气体的浓度与时间的关系如图乙所示。5min内,CO的平均反应速率![]() =_________________mol/(L?min)。
=_________________mol/(L?min)。
(2)下列措施中能使平衡时![]() 增大的是__________(填序号)。
增大的是__________(填序号)。
a.升高温度 b.增大压强 c.充入一定量CO d.再加入一些铁粉
(3)高铁酸钠是一种强氧化剂,具有广泛的用途。
①高铁酸钠与锌组成的高铁电池,不产生污染物,电压高、电量大,是广受欢迎的新型电源,该电池反应为:![]()
![]()
![]()
![]() ,请回答:放电反应为_________(填“反应①”或“反应②”),充电时阳极电极反应式为:_____________________________________。
,请回答:放电反应为_________(填“反应①”或“反应②”),充电时阳极电极反应式为:_____________________________________。
②高铁酸钠是一种新型饮用水净水消毒剂,请简述其净水消毒原理。
查看答案和解析>>
科目: 来源: 题型:
(16分)铜在自然界中存在于多种矿石中,如
| 矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 |
|
|
|
|
请回答以下问题:
(1)上表所列铜的化合物中,铜的质量分数最高的是______________(填化学式)。
(2)工业上以黄铜矿为原料,采取火法熔炼工艺生产铜。该过程中有如下反应:
![]() ,该反应的还原剂是____________;若在标准状况下放出气体56L,则转移电子的物质的量为_____________。
,该反应的还原剂是____________;若在标准状况下放出气体56L,则转移电子的物质的量为_____________。
(3)某同学采集酸雨样品并测其pH,发现在一段时间内其pH逐渐减小。请用必要的文字和化学方程式说明其原因______________________________________________
________________________________________________________。
(4)铜制品长期置于潮湿的环境中,表面会产生一层铜绿,其主要成分与孔雀石相同。
请写出采用化学方法除去铜器表面铜绿的有关反应的离子方程式:_____________
_______________________________________________。
(5)![]() 与
与![]() 都是红色粉末。
都是红色粉末。![]() 溶于稀
溶于稀![]() 会生成
会生成![]() 和
和![]() 。一同学为鉴定某
。一同学为鉴定某![]() 样品中是否混有多少量的
样品中是否混有多少量的![]() ,设计了如下实验:取少量粉末放入足量稀
,设计了如下实验:取少量粉末放入足量稀![]() 中,向所得溶液中滴加
中,向所得溶液中滴加![]() 试剂。该同学通过实验认为:若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含
试剂。该同学通过实验认为:若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含![]() 。你认为这种说法是否正确___________:简述你的理由(用离子方程式表示):______________,
。你认为这种说法是否正确___________:简述你的理由(用离子方程式表示):______________,
如果要得到准确的结论,还需加入的一种试剂是_________________。
查看答案和解析>>
科目: 来源: 题型:
常温下,![]() 的溶度积常数依次为:
的溶度积常数依次为:![]() 、
、
![]() 。下列有关说法中,错误的是
。下列有关说法中,错误的是
A.常温下,![]() 在水中溶解能力依次减弱
在水中溶解能力依次减弱
B.在![]() 饱和溶液中加入
饱和溶液中加入![]() 固体,有
固体,有![]() 沉淀生成
沉淀生成
C.![]() 的溶度积常数之比等于它们饱和溶液的物质的量浓度之比
的溶度积常数之比等于它们饱和溶液的物质的量浓度之比
D.在![]() 饱和溶液中加入
饱和溶液中加入![]() 固体有
固体有![]() 沉淀析出
沉淀析出
查看答案和解析>>
科目: 来源: 题型:
已知![]() 四种短周期主族元素在周期表中的相对位置如下图所示,下列说法正确的是
四种短周期主族元素在周期表中的相对位置如下图所示,下列说法正确的是
A.![]() 的原子序数可能是
的原子序数可能是![]() 的原子序数的2倍
的原子序数的2倍
B.![]() 元素的原子半径可能比
元素的原子半径可能比![]() 元素的小
元素的小
C.![]() 的气态氢化物的稳定性一定比
的气态氢化物的稳定性一定比![]() 的强
的强
D.![]() 的化学活泼性一定比
的化学活泼性一定比![]() 强
强

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com