
科目: 来源: 题型:
根据元素周期表1-20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有_______种,金属性最强的元素与氧反应生成的化合物有______________(填两种化合物的化学式);
(2)属于稀有气体的是_________(填元素符号,下同);
(3)形成化合物种类最多的两种元素是_______________________;
(4)第三周期中,原子半径最大的是(稀有气体除外)____________;
(5)推测Si、N最简单氢化物的稳定性_________大于__________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为______________________________________________。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___________________________。
(3)X的硝酸盐水溶液显____________性,用离子方程式解释原因:____________________。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_________________。
(5)比较Y、Z气态氢化物的稳定性:______________>____________。(用分子式表示)
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是_________>___________>____________>__________。
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量。写出该反应的热化学方程式:_____________________________。
查看答案和解析>>
科目: 来源: 题型:
V、W、X、Y、Z是由周期表中1~20号部分元素组成的5种化合物,其中V、W、X、Z均为两种元素组成。上述5种化合物涉及的所有元素的原子序数之和等于35。它们之间的反应关系如下图:
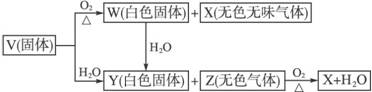
(1)5种化合物分别是V 、W 、X 、Y 、Z :(填化学式)
(2)由上述5种化合物中某2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是 :
(3)V的电子式是 。
查看答案和解析>>
科目: 来源: 题型:
Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于_____________晶体,俗名叫 ;
(2)R的氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是 ;
(3)X的常见氢化物的空间构型是 ;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是 ;
(4)Q分别与Y、Z形成的共价化合物的化学式是_____________和_________________;Q和Y形成的分子的电子式是_____________,属于 分子(填“极性”或“非极性”)。
查看答案和解析>>
科目: 来源: 题型:
氮是地球上极为丰富的元素。
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为 。
(2)N≡N的键能为942 kJ?mol-1,N-N单键的键能为247 kJ?mol-1。计算说明N2中的 键比 键稳定(填“![]() ”或“
”或“![]() ”)。
”)。
(3)(CH3)3NH+和![]() 可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂 (填“大”或“小”),可用作 (填代号)。
可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂 (填“大”或“小”),可用作 (填代号)。
a. 助燃剂
b.“绿色”溶剂
c. 复合材料
d. 绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是 ,与同一个N3-相连的X+有 个。

查看答案和解析>>
科目: 来源: 题型:
D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大,它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为 ;
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是 ,写出该元素的任意3种含氧酸的化学式: ;
(3)D和Y形成的化合物,其分子的空间构型为 ;
(4)D和X形成的化合物,其化学键类型属 ,其晶体类型属 ;
(5)金属镁和E的单质在高温下反应得到的产物是 ,此产物与水反应生成两种碱,该反应的化学方程式是 。
(6)试比较D和X的最高价氧化物熔点的高低并说明理由:
查看答案和解析>>
科目: 来源: 题型:
在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的化学式是__________;X与氢元素形成的化合物的电子式是_____________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是________________;D与E能形成一种非极性分子,该分子的结构式为________________;D所在族元素的氢化物中,沸点最低的是_________________________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是____________________________________。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z三者均为短周期元素,已知X元素有一种同位素不含中子,Y元素原子的最外层电子数是次外层电子数的2倍,Z元素原子的最外层电子数是次外层电子数的3倍。下列化学式①XYZ3、②X2YZ2、③X2YZ3、④X2Y2Z2、⑤X2Y2Z4、⑥X4Y2Z2中,并非都存在的一组分子是
A.①② B.④⑥ C.③⑤ D.②④
查看答案和解析>>
科目: 来源: 题型:
2007年诺贝尔化学奖得主Gerhard Ertl对金属Pt表面催化CO氧化反应的模型进行了深入研究。下列关于![]() Pt和
Pt和![]() Pt的说法正确的是( )
Pt的说法正确的是( )
A.![]() Pt和
Pt和![]() Pt的质子数相同,互称为同位素
Pt的质子数相同,互称为同位素
B.![]() Pt和
Pt和![]() Pt的中子数相同,互称为同位素
Pt的中子数相同,互称为同位素
C.![]() Pt和
Pt和![]() Pt的核外电子数相同,是同一种核素
Pt的核外电子数相同,是同一种核素
D.![]() Pt和
Pt和![]() Pt的质量数不同,不能互称为同位素
Pt的质量数不同,不能互称为同位素
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.SiH4比CH4稳定
B.O2-半径比F-的小
C.Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强
D.P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com