
科目: 来源: 题型:
下列电离方程式错误的是
A. CaCl2=Ca2++2Cl― B. K2SO4=2 K + +SO42―
C. HNO3=H++NO3― D. NaClO=Na++Cl-+O2―
查看答案和解析>>
科目: 来源: 题型:
小明体检的血液化验单中,葡萄糖为5.9×10-3mol/L。表示该体检指标的物理量是
A. 溶解度(s) B. 物质的量浓度(c) C. 质量分数(w) D.摩尔质量(M)
查看答案和解析>>
科目: 来源: 题型:
铋(Bi)在医药方面有重要应用。下列关于![]() Bi和
Bi和![]() Bi的说法正确的是
Bi的说法正确的是
A. 两者互为同位素 B. 两者都含有83个中子
C. 两者的核外电子数不同 D. 两者分别含有126和127个质子
查看答案和解析>>
科目: 来源: 题型:
根据中央电视台报道,近年来我国的一些沿江和沿海城市多次出现大雾天气致使高速公路关闭,航班停飞。雾属于下列分散系中的
A. 溶液 B. 悬浊液 C. 乳浊液 D. 胶体
查看答案和解析>>
科目: 来源: 题型:
为了测定乙醇的分子结构,有人设计了如图所示的用无水乙醇与钠反应并测定H2的体积的实验装置。回答下列有关问题:
(1)乙醇与钠反应的化学方程式: (2)按图将仪器装配好,降低C管,使B、C两管间出现15~20cm水位差异后停止。该操作的目的是 _______________________________________ 。
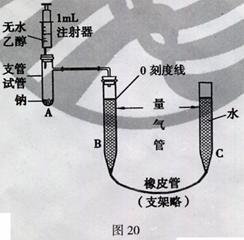
(3)已知无水乙醇密度在0.789g/mL,现取0.5mL无水乙醇,将0.25mL无水乙醇慢慢推入A中,使之与钠充分反应,则A中至少应加入钠的质量为 。(小数点保留一位数字)。
(4)注射器中吸入0.5mL无水乙醇,将称好的钠放入A中,在将乙醇推入A中之前,对量气管应该进行的操作是 。
(5)该实验装置与教材中实验装置相比,优点有 (填出两点即可)。
查看答案和解析>>
科目: 来源: 题型:
75℃左右在有催化剂作用下,乙炔可水化为乙醛。但催化剂遇到某些特定物质(如硫化氢)常会发生催化剂中毒而失去催化作用。现用如下装置图(仪器的支架已略去)制乙醛,请回答以下问题:
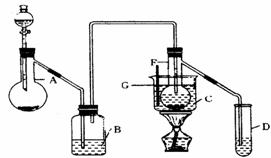
⑴试验开始时,仪器A中放入电石,为了使乙炔气流平稳,分液漏斗中常加入___________代替水;B中应装入______,其作用是_______ ________。
⑵ 装置图中,加热F时所选用的温度计G的量程表示正确的是__ ______(填代号)。
A、0―50℃ B、0―100℃ C、0―200℃ D、0―360℃
⑶本试验常用HgSO4做催化剂;现实验室只有浓硫酸、水、氧化汞粉末,若将三者分别直接加入蒸馏烧瓶F中,应先将_________________加入到F中,其操作方法是___________________;再按先后顺序分别将____________和_______________加入到F中。
⑷D中盛有水,用来吸收生成的乙醛。常用银镜反应来检验乙醛的存在,请写出该反应的化学方程式:___________________
在试验过程中,银镜将在试管的_________(填“上部”、“中部”、“下部”)首先出现;实验结束后,需用_____________清洗试管。
查看答案和解析>>
科目: 来源: 题型:阅读理解
本题有I和II两小题。
Ⅰ.下面a~e是中学化学实验中常见的几种定量仪器:
(a)量筒 (b)容量瓶 (c)滴定管 (d)托盘天平 (e)温度计
(1)其中标示出仪器使用温度的是__________(填写编号)。
(2)能够用以精确量取液体体积的是_______(填写编号)。
(3)由于操作错误,使得到的数据比正确数据偏小的是________(填写编号)。
A.用量筒量取一定量液体时,俯视液面读数
B.中和滴定达终点时俯视滴定管内液面读数
C.使用容量瓶配制溶液时,俯视液面定容所得溶液的浓度
(4)称取10.5 g固体样品(1 g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为_________g。
(5)有下列实验:
①苯与溴的取代反应 ②苯的硝化反应
③乙醛的银镜反应 ④测定一定温度下KNO3的溶解度
⑤乙酸乙酯的制取 ⑥石油分馏实验
其中需要使用温度计的有___________(填写编号)
Ⅱ.某种胃药片的制酸剂为碳酸钙,其中所含的CaCO3质量的测定如下:
①需配制0.1 mol/L的HCl和0.1 mol/L的NaOH溶液;
②每次取一粒(药片质量均相同)0.2 g的此胃药片,磨碎后加入20.00 mL蒸馏水;
③以酚酞为指示剂,用0.1 mol/L的NaOH溶液滴定,需用去V mL达滴定终点;
④加入25.00 mL 0.1 mol/L的HCl溶液。
(1)写出实验步骤(写编号顺序)___________________________。
(2)在下图所示的仪器中配制0.1 mol/L的HCl溶液和0.1 mol/L的NaOH溶液肯定不需要的仪器是(填序号)________,配制上述溶液还需要的玻璃仪器是(填仪器名称)_________________________。

(3)配制上述溶液应选用的容量瓶规格是_________(填字母)。
A.50 mL 50 mL B.100 mL 100 mL
C.100 mL 150 mL D.250 mL 250 mL
(4)写出有关的化学方程式______________。
(5)每片胃药中含碳酸钙的质量是____________________g。
查看答案和解析>>
科目: 来源: 题型:
钙是人体神经、骨骼系统等功能正常运作所必需的常量元素。某药业公司生产的钙片包装上有如下说明:
| 性状 | 本品为白色片 |
| 贮藏 | 密封,干燥处保存 |
| 规格 | 每片含碳酸钙0.5 g (相当于钙 0.2 g) |
| 包装 | 固体药用塑料瓶包装,每瓶100片 |
| 生产批号 | |
| 生产日期 | |
| 有效期至 |
某学习小组为了确定钙片中碳酸钙的含量是否符合包装说明上的规格,进行如下实验:
①取一片钙片研碎后加入足量稀盐酸,充分反应后过滤并洗涤。
②取①中滤液加入足量的(NH4)2C2O4溶液,使Ca2+全部转化为CaC2O4沉淀,过滤并洗涤。
③取②中沉淀完全溶于强酸中,得到草酸(H2C2O4),并稀释成1.000 L溶液。
④取③中溶液20.00 mL ,用0.0050 mol/L酸性高锰酸钾溶液滴定,恰好完全反应时,消
耗了12.00mL酸性高锰酸钾溶液,反应的离子方程式是(未配平)
_____MnO4-+_____H2C2O4+_____H+――_____Mn2++_____CO2↑ +______ H2O
(1)配平该反应的离子方程式(将化学计量数填于空白处)。
(2)过滤操作中需要用到的玻璃仪器的名称是___________________________。
(3)简述步骤②中沉淀是否洗涤干净的方法(写出操作、现象和结论):___________________________________________________________________________。
(4)滴定时是否需要指示剂?_________(填“是”或“否”),理由是___
(5)学习小组根据以上实验,计算出钙片中含碳酸钙的质量是___________g/片,与包装说明相比较,分析产生该实验结果可能的原因是_________________
查看答案和解析>>
科目: 来源: 题型:阅读理解
甲、乙、丙、丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞溶液,溶液变成了红色,一会儿红色就消失了。
[猜想]甲:可能是酚酞变质造成的;
乙:可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故;
丙:可能是酚酞与空气中的氧气反应,使红色消失;
丁:可能与氢氧化钠溶液质量分数大小有关。
[理论分析]
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是:
。
(2)丙同学认为乙同学的猜想也不正确,他的理由是
。
[实验设计]
(3)为证实丙同学的猜想,还需做如下实验,请完成下表:
| 实验步骤 | 设计这一步骤的目的 |
| 1.将配制的氢氧化钠溶液加热 | ① |
| 2.在加热后的溶液中滴加酚酞,并在上方滴一些植物油 | ② |
(4)通过以上实验,四位同学看到:溶液先变成红色,一会儿红色仍然消失。因此酚酞红色褪去与氧气无关。若丁同学的猜想正确,设计如下实验证明并完成有关问题:
| 实验方法 | 观察到的现象和结论 |
| 方案一:分别配制不同质量分数的氢氧化钠溶液,然后各滴加数滴酚酞溶液。 | 质量分数大的溶液中酚酞红色会消失,则证明 ① |
| 方案二:向原红色消失的溶液中加 ② (填试剂名称) | 红色重新出现,则说明红色消失与氢氧化钠溶液质量分数大小有关。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com