
科目: 来源: 题型:
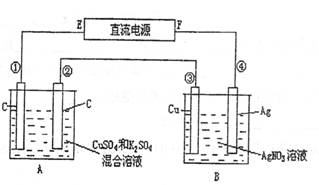
(4分)如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,设A池中原混合液的体积为200mL,求通电前A池原混合溶液中Cu2+的浓度。
查看答案和解析>>
科目: 来源: 题型:
(7分)在测定硫酸铜晶体中结晶水的含量的实验操作中:
(1)加热前晶体应该放在 中研碎,加热时是放在 中进行,加热失水后,应放在 中冷却。
(2)判断是否完全失水的方法是 。
(3)做此实验时,最少应该进行称量操作 次。
(4)下面是某学生一次实验的数据,请完成计算,填入下面的表中。
坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体的总质量 | 测得晶体中结晶水个数 |
11.7g | 22.7g | 18.6g |
|
(5)这次实验中产生误差的原因可能是(填选项)
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却
查看答案和解析>>
科目: 来源: 题型:
(8分)某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
![]()

(1)请将Au2O3之外的反应物与生成物分别填入以下空格内,并标出电子转移的方向和数目。
![]()
![]()
![]() (2)反应中,被还原的元素是 ,还原剂是 。
(2)反应中,被还原的元素是 ,还原剂是 。
![]() (3)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂物质的量之比为 。
(3)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂物质的量之比为 。
查看答案和解析>>
科目: 来源: 题型:
(9分)X、Y、Z三种元素,X与氢能形成气态XH4,其中X的质量分数为75%,且X与Y能形成XY2型化合物。Y的核内质子数和中子数相等 ,在Y的氢化物中,Y的质量分数为88.9%,Z是最高价氧化物的水化物是酸性最强的酸。
(1)X元素所形成的同素异形体中硬度最大的是 (填名称),它属于 晶体。
(2)Y的氢化物属于 晶体,它的电子式是 。
(3)Z元素位于周期表第 周期第 族,它的氢化物是 (填“极性”或“非极性”)分子。
![]() (4)X与Z形成的化合物其分子的空间构型是 ,它的晶体属于 晶体。
(4)X与Z形成的化合物其分子的空间构型是 ,它的晶体属于 晶体。
查看答案和解析>>
科目: 来源: 题型:
(12分)电解原理常应用于工业生产
(1)火法炼铜得到的粗铜中含多种杂质(如锌、金、银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯。在电解精炼时,粗铜接电源 极,电极反应为 ;纯铜作 极,电极反应为 。
(2)工业上用电解饱和食盐水的方法可制得烧碱、氯气、氢气。电解时,总反应化学方程式为 ;电解时所需的精制食盐水,通常在粗盐水中加入某些试剂来除去其中的Ca2+、Mg2+、Fe3+、SO42-杂质离子,添加试剂的先后顺序 (填所加试剂的化学式)。
(3)为了避免产物相混合发生副反应,工业上采用离子交换膜法电解食盐水。下图为阳离子交换膜法电解饱和食盐水 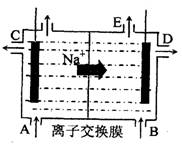 原理示意图。电极反应为:
原理示意图。电极反应为:
阳极 ,
阴极 。
下列说法中正确的是
A.从E口逸出的气体是H2
B.从B中加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4L Cl2,便产生2mol NaOH
D.向电解后的阳极室溶液中加适量盐酸,可以恢复到电解前的物质的浓度
查看答案和解析>>
科目: 来源: 题型:
(7分)已知H2O2分子的结构如图所示:H2O2分子不是直线型,两个H原子犹如在半展开的书的两页上,O原子则在书的 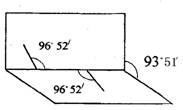 夹缝上,书页夹角为93°51′,
夹缝上,书页夹角为93°51′,![]() 而两个O―H键与O―O键的夹角均为96°52′。试回答:
而两个O―H键与O―O键的夹角均为96°52′。试回答:
![]() (1)写出H2O2分子的结构式 。
(1)写出H2O2分子的结构式 。
![]() (2)H2O2分子内含有 键(填“极性键”或“非极性键”)。
(2)H2O2分子内含有 键(填“极性键”或“非极性键”)。
(3)在下列反应中,体现了H2O2的哪些性质
![]() 2H2O2==2H2O+O2↑ 。
2H2O2==2H2O+O2↑ 。
![]() H2O2+SO2== H2SO4 。
H2O2+SO2== H2SO4 。
![]() H2O2+Cl2==2HCl+O2 。
H2O2+Cl2==2HCl+O2 。
![]() Na2O2+2HCl==H2O2+2NaCl 。
Na2O2+2HCl==H2O2+2NaCl 。
查看答案和解析>>
科目: 来源: 题型:
下列关于实验现象的描述不正确的是
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片做阳极,铁片做阴极,电解氯化锌溶液时,锌片溶解,电极反应:Zn-2e-=Zn2+
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入氯化铜溶液,气泡放出速率加快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com