
科目: 来源: 题型:
(08嘉定区期末)从右图所示的某气体反应的能量变化分析,以下判断错误的是 ()
 A.这是一个放热反应
A.这是一个放热反应
B.该反应可能需要加热
C.生成物的总能量低于参加反应的物质的总能量
D.反应物比生成物更稳定
查看答案和解析>>
科目: 来源: 题型:
(08黄埔区4月模拟)合成氨工业对国民经济和社会发展具有重要的意义。哈伯法合成氨需要在20-50MPa的高压和500℃的高温下,并用铁作为催化剂,氨的转化率为10%-15%;最近美国俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)2的催化剂,在常温下合成出氨。下列有关说法中错误的是()
A.哈伯法合成氨是吸热反应,新法合成氨是放热反应
B.新法合成和哈伯法相比不需要在高温条件下,可节约大量能源
C.新法合成能在常温下进行是因为不需要断裂化学键
D.新的催化剂降低了反应所需要的能量
查看答案和解析>>
科目: 来源: 题型:
(08闽行区模拟)2007年10月党的十七大报告中提出:形成节约能源和保护生态环境的产业结构是人类与自然和谐发展的重要保证。你认为下列行为中有悖于这一观点的是()
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.在农村大力推广和使用沼气
D.减少资源消耗、增加资源的重复使用和资源的循环再生
查看答案和解析>>
科目: 来源: 题型:
(08松江区第一期末)在一个固定体积为2升的密闭容器中,充入2 mol A和1 mol B,发生如下反应:2A(g) + B(g) ![]() 3C(g) + D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
3C(g) + D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
(1)写出该反应平衡常数的表达式 ,
2分钟内B 的平均反应速度为
(2)若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为________(填“吸热”或“放热”)反应。
(3)若将容器体积缩小至1升,反应达到平衡时C的浓度为 mol?L-1,
平衡常数 (填增大、减小或不变)
查看答案和解析>>
科目: 来源: 题型:
(08松江区第一期末)在一定温度下,可逆反应气A(气)+3B(气) ⇌ 2C(气)达到平衡的标志是()
A.C生成的速度是A反应速度的2倍
B.B、C的浓度不再变化
C. 单位时间内生成n摩A,同时生成3n摩B
D.A、B、C的分子数之比为1∶3∶2
查看答案和解析>>
科目: 来源: 题型:
(08松江区模拟)在密闭容器中,反应xA(g)+yB(g) ![]() zC(g),达到平衡后测得A气体的浓度为0.5 mol/L。保持温度不变,将密闭容器的容积增加一倍,当达到新的平衡时,测得A的浓度为0.3 mol/L,则下列叙述中正确的是( )
zC(g),达到平衡后测得A气体的浓度为0.5 mol/L。保持温度不变,将密闭容器的容积增加一倍,当达到新的平衡时,测得A的浓度为0.3 mol/L,则下列叙述中正确的是( )
A.平衡向正反应方向运动 B.x+y>z
C.物质C的体积分数增大 D.物质B的转化率增大
查看答案和解析>>
科目: 来源: 题型:
 (08松江区模拟)在一定温度时,N2与H2反应过程中能量变化的曲线如图。下列叙述正确的是( )
(08松江区模拟)在一定温度时,N2与H2反应过程中能量变化的曲线如图。下列叙述正确的是( )
A.该反应的热化学方程式为:N2+3H2![]() 2NH3+92kJ
2NH3+92kJ
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的放热增多
D.加入催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目: 来源: 题型:
(08松江区模拟)一定温度下,在体积为V L的密闭容器中,发生某可逆反应,其化学平衡常数表达式为:K=![]() 。
。
(1)写出该反应的化学方程式 ;
(2)若第t1 秒时,CO的物质的量为n mol,到第t2 秒时恰好达到平衡,此时CO的物质的量浓度为m mol/L,这段时间内的化学反应速率v(CO) = mol/L?s;
(3)向该平衡体系中通入一定量的H2,则平衡向 反应方向移动,平衡常数K
(填“增大”、“减小”或“不变”);
(4) 该反应的逆反应速率随时间变化的关系如图。
该反应的逆反应速率随时间变化的关系如图。
① 从图中看到,反应进行至t1时________ (填序号)
a.v(正)> v(逆) b.v(正) = v(逆) c.v(正) < v(逆)
② t1时改变了某种反应条件,改变的条件不可能
是_________(填序号)。
a.减小H2浓度 b.增大CO浓度 c.使用催化剂
查看答案和解析>>
科目: 来源: 题型:
(08黄埔区4月模拟)(8分)设反应①Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1 ,反应②Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1 ,反应②Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2 。在不同温度下,K1、K2的值如右表:
FeO(s)+H2(g)的平衡常数为K2 。在不同温度下,K1、K2的值如右表:
(1)从上表可以推断:反应①是_________(填“吸热”、“放热”)反应。
温度 | K1 | K2 |
973K | 1.47 | 2.38 |
1173K | 2.15 | 1.67 |
(2)要使反应②在一定的条件下建立的平衡向正反应方向移动,可采取的措施有______________(填写序号)。
A.缩小反应容器体积 B.扩大反应容器体积 C.降低温度
D.升高温度 E.使用合适的催化剂 F.设法减少H2的量
(3)下列图1、2表示反应①在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化
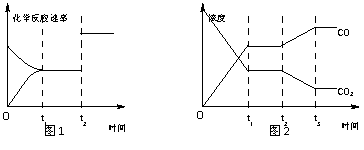 的情况:
的情况:
① 图1中时刻t2发生改变的条件是___________________________________。
② 图2中时刻t2发生改变的条件是___________________________________。
(4)若反应②在20L密闭容器中进行,当在一定条件下从反应开始经过5秒达到化学平衡,经测定氢气的体积为13.44升(已折合成标准状况),则用氢气表示该反应从开始到平衡时的平均反应速率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com