
科目: 来源: 题型:
(08浙江九所重点中学调研)下列物质提纯的方法正确的是()
A.除去混在NO2中的NO:将气体与过量O2混合
B.除去混在CO2中的SO2:将气体依次通过足量酸性KMnO4溶液和浓硫酸
C.除去KCl溶液中的K2CO3:加入过量BaCl2溶液后过滤
D.除去乙酸中混有的乙醇:向混合液中加入生石灰后蒸馏
查看答案和解析>>
科目: 来源: 题型:
(08杭州市质检)物质的分离是化学研究中常用的方法,填写下列物质分离时需使用的方法(不必叙述操作细节)。
(1)两种互不相溶的液体的分离 ▲ 。
(2)固体和液体的分离 ▲ 。
(3)含固体溶质的溶液中除去部分溶剂 ▲ 。
(4)胶体中分离出可溶电解质 ▲ 。
(5)几种沸点相差较大的互溶液体的分离 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
近年来,工业上用Mg(NO3)2代替浓H2SO4作为制取浓硝酸的吸水剂(以下数据为溶质质量分数)。65%的硝酸(质量为M1)中加入72%的Mg(NO3)2溶液(质量为M2)后蒸馏,分别得到97.5%的硝酸和60%的Mg(NO3)2溶液(不含有硝酸)。
(1)若蒸馏过程中,硝酸、Mg(NO3)2和水均无损耗,求蒸馏前的投料比M1/M2值__________。
(2)若蒸馏过程中,水的损耗占总质量(M1+M2)的5.0%,则投料时,比值M1/M2__________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
实验室制取SO2的反应原理为:Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
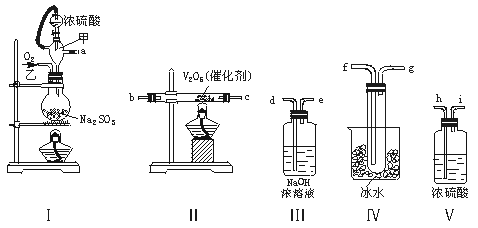
(1)这些装置的连接顺序(按气体左右的方向)是 → → → →
→ → → (填各接口的编号)。
(2)实验时甲仪器的作用与原理是 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。
(4)Ⅳ处观察到的现象是 。
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会 (填“增大”“不变”或“减小”)。
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为 。
查看答案和解析>>
科目: 来源: 题型:
(08杭州五校月考)某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种组成。取该溶液进行如下实验:
(A)取试液适量,加入过量稀盐酸,有气体生成,得到溶液甲;
(B)向溶液甲中再加入过量碳酸氢铵溶液,有气体生成,析出白色沉淀乙,得到溶液丙;
(C)向溶液丙中加入过量Ba(OH)2溶液,有气体生成,析出白色沉淀丁。
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是 。(全对才给分)
(2)一定存在的离子是 。(全对才给分)
(3)生成沉淀乙的离子反应方程式是 。
(4)写出步骤(C)中一定会发生反应的离子方程式 。
查看答案和解析>>
科目: 来源: 题型:
(08浙江金丽衢十二校联考) (10分)根据测定硫酸铜晶体中结晶水含量的实验,填写下列空白:
⑴ 有下列仪器,本实验中需要的仪器是(填写字母)___________________________,除上述仪器外,还需要的仪器是(填仪器名称): ________________________________。
A、带砝码的托盘天平 B、研钵 C、试管夹 D、酒精灯 E、蒸发皿
F、玻璃棒 G、坩埚 H、干燥管 I、石棉网 J、三角架
⑵ 本实验至少需要加热_____________次,至少需要称量__________次;
⑶ 某学生实验得到以下数据:加热前容器的质量为m1,容器和晶体的总质量为m2,加热后容器和无水CuSO4的总质量为m3。请写出结晶水含量(ω)的计算公式并求出CuSO4?nH2O中n的值(用ml、m2、m3表示): ω= ____________________,n = _____________________
⑷ 若ml = 5.4g、m2 = 7.9g、m3 = 6.8g,该生测得实验结果偏高还是偏低? _______________
从下列分析中选出该生实验产生误差的原因可能是(填写字母) ___________________
A、加热前称量时容器未完全干燥 B、最后两次加热后的质量差大于0.1g
C、加热后容器未放在干燥容器中冷却 D、加热过程中有少量晶体溅出
E、加热后的粉末中有少量黑色固体
查看答案和解析>>
科目: 来源: 题型:
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为 。
(2)漂白粉的有效成分是(填化学式) 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 。
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号) 。
查看答案和解析>>
科目: 来源: 题型:
SO2和Cl2都具有漂白性,若将等物质的量的这两种气体同时作用于潮湿的有色物质,可观察到有色物质
A.立刻褪色 B.慢慢褪色 C.先褪色,后复原 D.颜色不褪
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com