
科目: 来源: 题型:
工厂的工业废水,不可直接往江河排放,否则会造成严重公害。某河道两旁有甲、乙两厂,它们排出的工业废水各含有K+、Fe3+、Ba2+、Ag+、Cl-、SO42-、NO3-、
OH-中的四种。又知甲厂污水pH>7。
(1)甲厂污水中含有的四种离子可能是:_____________________________________。
(2)乙厂污水中含有的四种离子可能是:_____________________________________。
(3)乙厂进行废水处理,方法之一,可往废水中加入一定量的_______________(选填;活性炭、硫酸亚铁、铁粉),可以回收其中的金属___________________(填元素符号)。
(4)消除污染的另一种重要措施是将甲、乙两厂的废水按比例混合,可使废水中的___________(填离子符号)转化为沉淀,再排放则大大降低污染程度。过滤,所得废水主要含_______________________,可用于浇灌农田。
查看答案和解析>>
科目: 来源: 题型:
向饱和的Na2CO3溶液中通入过量的CO2气体,现象是______________________,产生此现象的原因是___________________________________.
查看答案和解析>>
科目: 来源: 题型:
我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
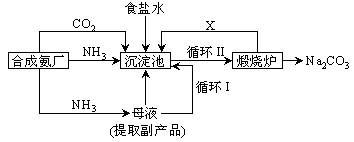
(1) 上述生产纯碱的方法称 ,副产品的一种用途为 。
(2) 沉淀池中发生的化学反应方程式是 。
(3) 写出上述流程中X物质的分子式 。
(4) 使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是 。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 。
(6) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 。
(a) 增大NH4+的浓度,使NH4Cl更多地析出 (b) 使NaHCO3更多地析出
(c) 使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
查看答案和解析>>
科目: 来源: 题型:
化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡.
NH3+H2O ![]() NH3?H2O
NH3?H2O ![]() NH4++OH-
NH4++OH-
(1)向氨水中加入MgCl2固体时,平衡向__________移动,OH-的浓度__________,NH4+的浓度_____。
(2)向氨水中加入浓盐酸,平衡向___________移动,此时溶液中浓度减小的粒子有___________、___________、___________。
(3)向浓氨水中加入少量NaOH固体,平衡向______移动,此时发生的现象 __________。
查看答案和解析>>
科目: 来源: 题型:
工业上用氨和二氧化碳反应合成尿素,其反应是:CO2+2NH3=CO(NH2)2+H2O。已知下列物质在一定条件下均能与水反应产生H2和CO2。H2是合成氨的原料,CO2供合成尿素用。
(1)若从充分利用原料的角度考虑,选用 (填序号)作原料较好。
A. CO B. 石脑油(C5H12、C6H14) C. CH4 D. 焦炭
(2)作出这种选择的依据是 。
注:有关的反应如下:① C+2H2O=CO2+2H2 ② CO+H2O=CO2+H2
③ CH4+2H2O=CO2+4H2 ④ C5H12+10H2O=5CO2+16
查看答案和解析>>
科目: 来源: 题型:
除去下列溶液中混有的少量杂质(括号内的物质),应加入什么试剂?写出有关反应的离子方程式.
(1)NaOH (Na2CO3)
(2)NaNO3 (NaCl)
(3)Na2CO3 (NaHCO3)
查看答案和解析>>
科目: 来源: 题型:
已知N![]() (g)+3H
(g)+3H![]() (g)
(g)![]() 2NH
2NH![]() (g)
(g) ![]() ,
,
2SO![]() (g)+O
(g)+O![]() (g)
(g)![]() 2 SO
2 SO![]() (g)
(g) ![]() 。回答下列问题:
。回答下列问题:
(1)从影响速率和平衡的因素分析,要有利于NH![]() 和SO
和SO![]() 的生成,理论上应采取的措施是_______________,实际生产中采取的措施分别是_____________、________________。
的生成,理论上应采取的措施是_______________,实际生产中采取的措施分别是_____________、________________。
(2)在实际生产合成氨过程,要分离出氨气,目的是_____________;而合成SO![]() 过程中,不需要分离出SO
过程中,不需要分离出SO![]() ,原因是_____________。
,原因是_____________。
查看答案和解析>>
科目: 来源: 题型:
在一定温度和压强下,合成氨反应达到平衡时,下列操作平衡不发生移动的是
A、恒温、恒压时充入氨气 B、恒温、恒容时充入氮气
C、恒温、恒容时充入氦气 D、恒温、恒压时充入氦气
查看答案和解析>>
科目: 来源: 题型:
合成氨的温度和压强通常控制在约![]() C
C![]() 和H
和H![]() 的体积比为1:3,经科学测定,在相应条件下,N
的体积比为1:3,经科学测定,在相应条件下,N![]() 和H
和H![]() 反应所得氨的平衡浓度(体积分数)如下表所示。而实际从合成塔出来的混合气体中含有氨约为15%,这表明
反应所得氨的平衡浓度(体积分数)如下表所示。而实际从合成塔出来的混合气体中含有氨约为15%,这表明
| 200atm | 600atm |
| 19.1% | 42.2% |
A、表中所测数据有明显误差 B、生产条件控制不当
C、氨的分解速率大于预测值 D、合成塔中的反应并未达平衡
查看答案和解析>>
科目: 来源: 题型:
在某化学平衡中,改变温度(其他条件不变),![]() ,随着时间的推移,在新条件下建立起新的平衡,此时反应物的浓度一定
,随着时间的推移,在新条件下建立起新的平衡,此时反应物的浓度一定
A.大于生成物浓度
B.小于生成物浓度
C.与生成物浓度相等
D.大于原平衡时该物质的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com