
科目: 来源: 题型:
根据以下叙述回答①和②题。
把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:
3X(g)+Y(g)=nZ(g)+2W(g),5min末已生成0.2molW,若测知以Z浓度变化来表示的反应平均速率为0.01mol?L-1?min-1,则
②上述反应在5min末时,已作用去的Y值占原来量的物质的量分数
A.20% B.25% C.33% D.50%
查看答案和解析>>
科目: 来源: 题型:
根据以下叙述回答①和②题。
把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:
3X(g)+Y(g)=nZ(g)+2W(g),5min末已生成0.2molW,若测知以Z浓度变化来表示的反应平均速率为0.01mol?L-1?min-1,则
①上述反应中Z气体的化学计量数n的值是
A.1 B.2 C.3 D.4
查看答案和解析>>
科目: 来源: 题型:
反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
A.容器内压强不再变化 B.Fe3O4的物质的量不变
C.v(H2O)=v(H2) D.反应不再进行
查看答案和解析>>
科目: 来源: 题型:
(08安徽萧县中学模拟)实验室用50 mL 1.0 mol?L-1盐酸跟50 mL 1.1 mol?L-1氢氧化钠溶液在下图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题:
⑴大小烧杯间填满碎泡沫塑料的作用是 。
 ⑵ (填“能”或“不能”)将环形玻璃搅拌棒改为环形金属(如铜)棒。其原因是 。
⑵ (填“能”或“不能”)将环形玻璃搅拌棒改为环形金属(如铜)棒。其原因是 。
⑶大烧杯上如不盖硬纸板,对求得中和热数值的影响是 (填“偏高”或“偏低”或“无影响”)。
⑷如果改用60 mL 1.0 mol?L-1盐酸跟50 mL 1.1 mol?L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量 (“增加”、 “减少”或“不变”),理由是 ;
所求中和热数值 (“增加”、 “减少”或“不变”),理由是 。
查看答案和解析>>
科目: 来源: 题型:
(08安师大附中二模)已知在1×105 Pa,298 K条件下,2 mol氢气燃烧生成水蒸气放出484 KJ热量,下列热化学方程式正确的是 ( )
A. H2O(g) == H2(g)+1/2 O2(g); △H1=+242 kJ?mol-1
B. 2 H2(g)+ O2(g)===2 H2O(l); △H2=- 484 kJ?mol-1
C. H2(g)+1/2 O2(g)====H2O(g) ; △H1=+242 kJ?mol-1
D. 2 H2(g)+ O2(g)===2 H2O(g); △H2=+484 kJ?mol-1
查看答案和解析>>
科目: 来源: 题型:
t℃时,将3 mol A和1 mol B气体通人体积为2L的密闭容器中(容积不变),发生如下反应:3 A(g)+B(g) ![]() xC(g),2min时反应达到平衡状态(温度不变),剩余了O.8 mol B,并测得C的浓度为O.4 mol/L,请填写下列空白:
xC(g),2min时反应达到平衡状态(温度不变),剩余了O.8 mol B,并测得C的浓度为O.4 mol/L,请填写下列空白:
(1)从开始反应至达到平衡状态,生成C的平均反应速率为 ;
(2)x=_______;
(3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母)
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(4)若向原平衡混合物的容器中再充人a mol C,在t℃时达到新的平衡,此时B的物质的量为n(B)= mol;
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为 。
查看答案和解析>>
科目: 来源: 题型:
2007年5月31日是第二十个世界无烟日,主题是“创建无烟环境”,烟草是造成人类死亡的第二大原因。中国人每年消费世界上1/3的香烟。吸烟有害健康,烟草不完全燃烧时产生的一氧化碳被吸进肺里跟血液中的血红蛋白(用Hb表示)化合,发生下述反应:CO+Hb?O2 ![]() O2+Hb?CO,实验表明,Hb?CO的浓度即使只有Hb?02浓度的2%,也足以使人智力受损。当过多的血红蛋白与一氧化碳结合时,会引起窒息而死亡。
O2+Hb?CO,实验表明,Hb?CO的浓度即使只有Hb?02浓度的2%,也足以使人智力受损。当过多的血红蛋白与一氧化碳结合时,会引起窒息而死亡。
(1)化学平衡常数K表示可逆反应的进行程度,上述反应K= _________________ ,K值越大,表示_________________, K值大小与温度的关系是:温度升高,K值______________ (填“一定增大、一定减小、或可能增大也可能减小”)。
(2) Hb与CO通过什么化学键结合成Hb?CO分子的? 并判断Hb?CO分子与Hb?02分子的稳定性强弱
(3)抽烟后,吸入肺部的空气测得CO和02的浓度分别为10-6mol/L和10-2mol/L。已知37℃时,平衡常数K=220,这时Hb?CO的浓度是Hb?02浓度的________倍?这时候是否达到损伤人的智力的程度?试通过计算回答。
查看答案和解析>>
科目: 来源: 题型:
甲、乙两容器,甲的容积固定,乙的容积可变。在一定温度下,向甲中通入3mol N2和4mol H2,反应达到平衡时,生成NH3的物质的量为a mol。
(1)在相同温度下,向乙中通人2mol NH3,且保持容积与甲相同,当反应达到平衡时,各物质的浓度与甲中平衡相同。起始时乙中还应通入 mol N2和 mol H2
(2)相同温度下,若乙中通人6mol N2和8mol H2,且保持压强与甲相同,当反应达到平衡时,生成氨的物质的量为b mol,则a/b 1/2;若乙与甲的容积始终相等,达到平衡时,生成氨的物质的量为c mol,则a/c 1/2 (填 “<”,或“=”,或“>”)。
查看答案和解析>>
科目: 来源: 题型:
(08安徽模拟)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
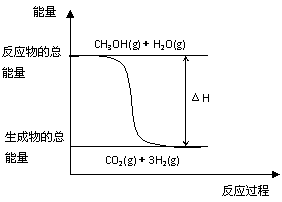
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= + 49.0 kJ?mol-1
②CH3OH(g)+O2(g)=CO2(g)+2H2(g); △H=-192.9 kJ?mol-1
下列说法正确的是( )
A.CH3OH的燃烧放出192.9 kJ?mol-1的量
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ?mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com