
科目: 来源: 题型:
室温下,在pH=12的某溶液中,由水电离的c(OH-)为
A.1.0×10-7 mol?L-1 B.1.0×10-6 mol?L-1
C.1.0×10-2 mol?L-1 D.1.0×10-12 mol?L-1
查看答案和解析>>
科目: 来源: 题型:
将纯水加热至较高温度,下列叙述正确的是
A.水的离子积变大、pH变小、呈酸性 B.水的离子积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性 D.水的离子积变大、pH变小、呈中性
查看答案和解析>>
科目: 来源: 题型:
(08安徽六校联考)(18分)某同学设计下列装置进行铁和浓H2SO4反应的实验探究,请回答下列问题。
(1)将16克铁粉放入烧瓶中,由分液漏斗放入18mol/L的浓H2SO420mL,结果没有任何反应现象,原因是__随后点燃A处酒精灯,就有气体产生了(2分)
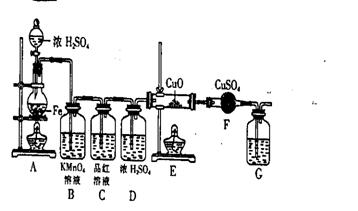 (2)随着反应的进行,B中酸性KMnO4溶液颜色逐渐变浅,请用离子方程式表示_______(3分)C中品红溶液颜色始终没有变化。
(2)随着反应的进行,B中酸性KMnO4溶液颜色逐渐变浅,请用离子方程式表示_______(3分)C中品红溶液颜色始终没有变化。
(3)当G处有持续稳定的气泡时,再点燃E处酒精灯,这样操作的原因是______3分)
(4)反应进行一段时间后,E、F处可观察到明显的现象,其中E中的反应方程式是___(3分),F处可看到的实验现象是___(3分)
(5)为了确保实验的严谨性和F中现象的可信性,G中盛放的液体可以是___________(4分)
A. CaCl2溶液 B. Ca(OH)2溶液 C. 浓硫酸 D. CCl4
查看答案和解析>>
科目: 来源: 题型:
已知25℃ 时几种物质的电离度(溶液的浓度为0.1mol/L)如下表:
①H2SO4溶液中的HSO4- | ②NaHSO4溶液中HSO4- | ③CH3COOH | ④HCl |
10% | 29% | 1.33% | 100% |
(1)25℃时,0.1mol/L上述几种溶液中c(H+)由大到小的顺序是 ;
(2)25℃时,pH值相同的上述几种溶液中物质的量浓度由大到小的顺序是 ;
(3)25℃时,将足量 Zn粉放入等体积、pH = 1的上述溶液中,产生H2的体积(同温同压下)由大到小的顺序是 ;
(4)25℃时,0.1mol/LH2SO4溶液中的HSO4-的电离度小于NaHSO4溶液中HSO4-的电离度的原因是 。
查看答案和解析>>
科目: 来源: 题型:
(08芜湖二模)对于Br2+2H2O+SO2=====2HBr+H2SO4和2HBr+H2SO4(浓)====Br2+2H2O+SO2↑的判断正确的是()
A.它们互为可逆反应
B.反应条件的改变,引起了反应方向的改变,都符合事实
C.氧化性H2SO4>Br2,还原性Br2>H2SO4
D.它们互相矛盾,不符合事实
查看答案和解析>>
科目: 来源: 题型:
双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式: 。
(2)鉴于H2O2显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出H2O2与Ba(OH)2作用形成盐的化学方程式: 。
(3)水电离生成 H3O+和 OH-叫做水的自偶电离。同水一样,H2O2也有极微弱的自偶电离,其自偶电离的方程式为: 。
查看答案和解析>>
科目: 来源: 题型:
对比同体积、同浓度的盐酸和醋酸,c(H+)前者 后者,与碱完全中和时,消耗NaOH的物质的量是前者 后者,与足量的Zn反应产生H2的速率是前者 后者,产生H2的量是前者 后者。(填“>”、“<”或“=”)
查看答案和解析>>
科目: 来源: 题型:
欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,其方法是
A.通入二氧化碳气体 B.加入氢氧化钠固体
C.通入氯化氢气体 D.加入饱和石灰水溶液
查看答案和解析>>
科目: 来源: 题型:
将0.1mol?L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起
A.溶液的pH增加 B.促进CH3COOH的电离
C.溶液的导电能力减弱 D.溶液中c(OH-)减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com