
科目: 来源: 题型:
(08上海12校联考)500℃、20Mpa时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中
H2、N2和NH3物质的量变化如图所示,根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=
此时增加N2的量,平衡常数将 (填“增大”
“减小”或“不变”)
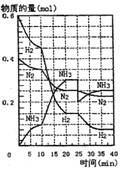
(2)500℃、20Mpa时,反应处于平衡状态的时间 。
(3)反应开始到第一次平衡时,N2的平均反应速率为 。
(4)据图判断,反应进行到10min至20min时曲线发生变化的原
因是: 反应进行至25min时,曲线发生变化的
原因是 。
查看答案和解析>>
科目: 来源: 题型:
室温时,0.01 mol?L-1某一元弱酸,则下列说法正确的是
A.上述弱酸溶液的pH=2
B.加入等体积0.01 mol?L-1 NaOH溶液后,所得溶液的pH=7
C.加入等体积0.01 mol?L-1 NaOH溶液后,所得溶液的pH>7
D.加入等体积0.01 mol?L-1NaOH溶液后,所得溶液的pH<7
查看答案和解析>>
科目: 来源: 题型:
室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是
A.0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液
B.0.1mol/L的盐酸和0.1mol/L的氢氧化钡溶液
C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液
D.pH=4的盐酸和pH=l0的氨水
查看答案和解析>>
科目: 来源: 题型:
(08上海嘉定区期末)甲烷蒸气转化反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g),工业上可利用
CO(g)+3H2(g),工业上可利用
此反应生产合成氨原料气H2。
已知温度、压强和水碳比[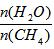 ]对甲烷蒸汽转化反应的影响如下图:
]对甲烷蒸汽转化反应的影响如下图:
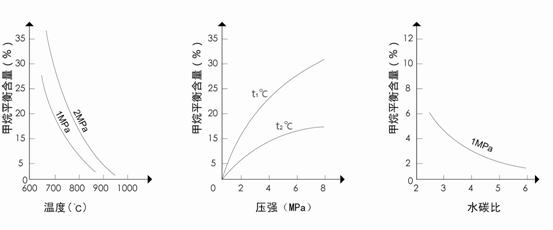
图1(水碳比为3) 图2(水碳比为3) 图3(800℃)
(1)该反应平衡常数K表达式为________________________。
(2)降低反应的水碳比平衡常数K__________(选填“增大”、“减小”或“不变”);
升高温度,平衡向____________方向移动(选正反应或逆反应)。
(3)图2中,两条曲线所示温度的关系是:t1_____t2(选填>、=或<);
图1中,在800℃、2MPa比1MPa时的甲烷含量_______(选填高、低或不变),
原因是____________________________________________________
(4)工业生产中使用镍作催化剂。但要求原料中含硫量小于5×10-7%,其目的是?
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.pH=2与pH=1的硝酸中c(H+)之比为1∶10
B.Na2CO3溶液中c(Na+)与c(CO32ˉ )之比为2∶1
C.0.2mol/L与0.1mol/L醋酸中c(H+)之比为2∶1
D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3∶1
查看答案和解析>>
科目: 来源: 题型:
物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是
A.Na2CO3 NaHCO3 NaCl NH4Cl
B.Na2CO3 NaHCO3 NH4Cl NaCl
C.(NH4)2SO4 NH4Cl NaNO3 Na2S
D.NH4Cl (NH4)2SO4 Na2S NaNO3
查看答案和解析>>
科目: 来源: 题型:
下列有关pH变化的判断中,正确的是
A.随着温度的升高,碳酸钠溶液的pH减小
B.随着温度的升高,纯水的pH增大
C.新制氯水经光照一段时间后,pH减小
D.氢氧化钠溶液久置于空气中,pH增大
查看答案和解析>>
科目: 来源: 题型:
已知反应 BeCl2+ Na2BeO2+ 2H2O![]() 2NaCl+ 2Be(OH)2↓能完全进行,则下列推断中,正确的是.
2NaCl+ 2Be(OH)2↓能完全进行,则下列推断中,正确的是.
A.BeCl2溶液的 pH < 7,将其蒸干并灼烧后,得到的残留物可能为 BeO
B.Na2BeO2溶液的 pH > 7,将其蒸干并灼烧后,得到的残留物可能为 BeO
C.Be(OH)2既能溶于盐酸又能溶于烧碱溶液
D .BeCl2水溶液的导电性强,因此BeCl2一定是离子化合物
查看答案和解析>>
科目: 来源: 题型:
某二元弱酸的酸式盐 NaHA 溶液,若 pH < 7 则溶液中各离子的浓度关系不正确的是
A .c(Na+)> c(HA-)> c(H+)> c(A2-)> c(OH-)
B.c(Na+)+ c(H+)= c(HA-)+ 2c(A2-)+ c(OH-)
C.c(H+)+ c(A2-)= c(OH-)+ c(H2A)
D .c(Na+)= c(HA-)+ c(H2A)+ c(A2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com