
科目: 来源: 题型:
(08泉州五中模拟)下列各项因果关系中正确的是( )
A.氨的沸点高于氯化氢,是因为分子间会形成氢键的氢化物其沸点一定高于不形成氢键的氢化物
B.同温下,强电解质溶液的导电能力一定大于弱电解质,是因为强电解质在溶液中完全电离
C.常温下,可用铁制容器装运浓硝酸,是因为常温下铁与浓硝酸不反应
D.苯酚钠溶液通入CO2后不生成Na2CO3,是因为HCO3-电离H+的能力弱于苯酚查看答案和解析>>
科目: 来源: 题型:
( 08鄞州中学限时训)下图是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构图是 ( )
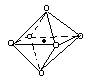 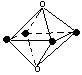 | 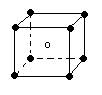 | 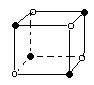 | |
⑴ ⑵ ⑶ ⑷
A.图⑴和图⑶ B.图⑵和图⑶ C.图⑴和图⑷ D.只有图(4)
查看答案和解析>>
科目: 来源: 题型:
( 08鄞州中学限时训)由解放军总装备部军事医学院研究所研制的小分子团水,解决了医务人员工作时的如厕问题。新型小分子团水,具有饮用量少、渗透力强、生物利用率高、在人体内储存时间长、排放量少的特点。一次饮用125mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是 ( )
A.水分子的化学性质改变 B.水分子中氢氧键缩短
C.水分子间的作用力减小 D.水分子间结构、物理性质改变
查看答案和解析>>
科目: 来源: 题型:
( 08鄞州中学限时训)下列说法正确的是 ( )
A.有些物质是由分子直接构成的,如二氧化碳、二氧化硫等;有些物质是由原子直接构成的,如金刚石、重晶石等;有些物质是由离子直接构成的,如食盐、纯碱等
B.分子是保持物质性质的一种微粒,也是化学变化中的最小微粒
C.N2O5 、N2O3、NO2不都是酸性氧化物;Na2O、Na2O2、Al2O3不都是碱性氧化物
D.H2O 是一种非常稳定的化合物,这是由于氢键所致
查看答案和解析>>
科目: 来源: 题型:
(08厦门市质检)在元素周期表中相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物除CH4外,还有C2H6等。运送飞船的火箭燃料有一种液态氮氢化合物。已知该化合物的相对分子质量为32,其中氢元素的质量分数为12.5%,分析发现该分子结构中只有单键。
(1)该氮氢化合物的电子式为 ,其沸点比氨__________ (填“高”或“低”),稳定性比氨__________ ( 填“好”或“差”)。
(2)若64g该氮氢化合物与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000kJ的热量。试写出该反应的热化学方程式: 。
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl NH4Cl。试写出上述氮氢化合物加入足量盐酸时,发生反应的化学方程式为 。
(4)氮原子间也可形成链状结构,假设氮原子间只以N-N键形式连接,并形成氢化物,则该系列氢化物的通式为 。
查看答案和解析>>
科目: 来源: 题型:
(08厦门市质检)下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是 ( )
A.SO2和SiO2 B.CO2和H2O C.NaC1和HC1 D.CC14和KC1
查看答案和解析>>
科目: 来源: 题型:
(08福州八中质检)三氯化氮(NCl3)在常温下是一种淡黄色液体,其分子呈三角锥形,以下关于NCl3的叙述正确的是( )
A.NCl3形成的晶体为原子晶体
B.分子中N-Cl键是非极性共价键
C.NCl3是一种含极性键的极性分子
D.N-Cl键能小,故NCl3沸点低
查看答案和解析>>
科目: 来源: 题型:
(08福州八中质检)根据相关的化学原理,下列判断正确的是( )
A.由于水中存在氢键,所以稳定性:H2O>H2S
B.由于二氧化硅的相对分子质量比二氧化碳的大,所以沸点:SiO2>CO2
C.若A2 + 2D― == 2A― + D2,则氧化性D2>A2
D.若R2―和M+的电子层结构相同,则离子半径R2―>M+
查看答案和解析>>
科目: 来源: 题型:
(08福州八中质检)下列有关氮气的叙述不正确的是: ( )
A.氮分子为非极性分子
B.在灯泡中充入氮气可防止钨丝被氧化
C.氮元素比磷元素非金属性强,因而氮气比磷的化学性质活泼
D.液氮可作冷冻剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com