
科目: 来源: 题型:
(08淄博调研)向存的大量Na+、C1-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是()
A.K+、Br-、CO32- B.A13+、H+、MnO4-
C.NH4+、Fe3+、SO42- D.Ag+、Ca2+、NO3-
查看答案和解析>>
科目: 来源: 题型:
(08威海市模拟)(8分)钢材厂家在生成钢材之后对其表面进行处理,形成一层致密的氧化物保护层;而使用厂家在对钢材进行加工使用前往往要除去钢材表面的氧化物,其中一种常见的方法是利用硫酸与钢材反应,此方法除去氧气的原理不是因为氧化物与酸反应,而是由于氧化物里面的金属铁与酸反应生成了氢气,使氧化物与金属分离脱落。但是在实际生产中工人师傅有几个问题请你帮助解决一下:
(1)下列哪种操作可以加快除去氧化物的速率 (填编号)
A.用浓硫酸 B.用中等浓度的硫酸
C.适当的提高温度 D.加少许铜屑
(2)反应的过程中溶液中 离子减少, 离子增加
(3)工业上在除氧化物过程中铁除了与硫酸反应外还与另一种离子反应,请写出离子方程式_______。
(4)为了减少废物,请你考虑可以从反应后的溶液中提取 物质。
提取分离时 → →趁热过滤
查看答案和解析>>
科目: 来源: 题型:
(08威海市质检)氨是重要的工农业生产原料,为了进一步提高合成氨的生产效率,在科研中的研究方向正确的是( )
A.研制耐高温、高压的新材料 B.研制低温下活性较大的催化剂
C.研制高温下活性较大的催化剂 D.寻求氮气、氢气的新来源
查看答案和解析>>
科目: 来源: 题型:
(08威海市质检)下列关于工业生产的说法中,不正确的是( )
A.工业上,用焦炭在电炉中还原二氧化硅得到含少量杂质的粗硅
B.生产普通玻璃的主要原料有石灰石、石英和纯碱
C.工业上将粗铜进行精炼,应将粗铜连接在电源的正极
D.在高炉炼铁的反应中,焦炭为氧化剂
查看答案和解析>>
科目: 来源: 题型:
(08山东省淄博模拟)(8分)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺,请按要求回答问题:
(1)“氨碱法”产生大量CaC12废弃物,请写出该工艺中产生CaC12的化学方程式:___________。
(2)写出“联合制碱法”有关反应的化验学方程式:____________。
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?________。
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:
原子利用率(%)= 。
查看答案和解析>>
科目: 来源: 题型:
(08山东一模)钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:_______。
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3•x H2O),反应的化学方程式:____________。
(3)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,
溶液中发生的化合反应的化学方程式______________________________。
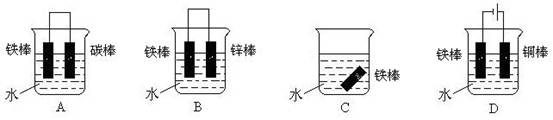
(4)下列哪个装置可防止铁棒被腐蚀_____________ 。
(5)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:

请回答:
① A电极对应的金属是______(写元素名称),B电极的电极反应式是 。
② 若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二
者质量差为5.12 g,则电镀时电路中通过的电子为________________mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因________。
查看答案和解析>>
科目: 来源: 题型:
(08山东二模)下列关于工业生产的说法中,不正确的是()
A.工业上,用焦炭在电炉中还原二氧化硅得到含少量杂质的粗硅
B.生产普通玻璃的主要原料有石灰石、石英和纯碱
C.工业上将粗铜进行精炼,应将粗铜连接在电源的正极
D.在高炉炼铁的反应中,焦炭为氧化剂
查看答案和解析>>
科目: 来源: 题型:
(07年江苏卷)下列说法正确的是()
A.原子晶体中只存在非极性共价键
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物一定是离子化合物
查看答案和解析>>
科目: 来源: 题型:
(08青岛检测)(8分) 聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n?XH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣――铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:
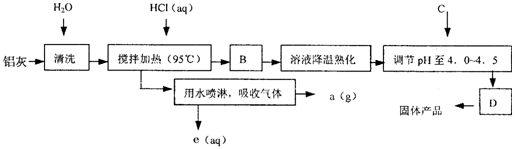
(1)搅拌加热操作过程中发生反应的离子方程式为:
; 。
(2)生产过程中B和D的操作名称分别是 和 (B和D均为简单操作)。
(3)反应中副产品a是 。
(4)生产过程中可循环使用的物质是 (用化学式表示)。
(5)调节pH至4.0~4.5的目的是 。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程C物质可选用 。
A.NaOH B.Al C.氨水 D.Al2O3 E.NaAlO2
查看答案和解析>>
科目: 来源: 题型:
(08青岛质检)(8分)现代社会中铜在电气、交通、机械和冶金、能源及石化工业、高科技等领域有广泛的应用。某铜矿石含氧化铜、氧化亚铜、三氧化二铁和脉石(SiO2),现采用酸浸法从矿石中提取铜,其工艺流程图如下。其中铜的萃取(铜从水层进入有机层的过程)和反萃取(铜从有机层进入水层的过程)是现代湿法炼铜的重要工艺手段。
|
已知:①Cu+在酸性溶液中不稳定,可发生自身氧化还原反应;②当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;③反萃取后的水层2是硫酸铜溶液。
回答下列问题:
(1)矿石用稀硫酸处理过程中Cu2O发生反应的离子方程式为: ;
(2)“循环I”经多次循环后的水层1不能继续循环使用,但可分离出一种重要的硫酸盐晶体,该晶体的化学式是 。若水层1暴露在空气中一段时间后,可以得到另一种重要的硫酸盐,写出水层1暴露在空气中发生反应的离子方程式 。
(3)写出电解过程中阳极(惰性电极)发生反应的电极反应式: 。
(4)“循环III”中反萃取剂的主要成分是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com