
科目: 来源: 题型:
下表列举的各组事实中存在因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 高纯单质硅具有半导体性能 | 高纯单质硅制成的光电池可将光能直接转化为电能 |
B | 钠原子核外电子数比铝少 | 钠的金属性比铝强 |
C | 氯的非金属性比碘强 | I2与KClO3反应生成Cl2和KIO3 |
D | N2+3H22NH3是放热反应 | 工业合成氨的反应在高温下进行 |
查看答案和解析>>
科目: 来源: 题型:
下列关于铁作电极的说法不正确的是
A.钢铁发生吸氧腐蚀时,铁作负极
B.利用牺牲阳极的阴极保护法防止钢铁腐蚀时,铁作正极
C.利用外加电流的阴极保护法防止钢铁腐蚀时,铁作阳极
D.在铁制品上电镀时,铁作阴极
查看答案和解析>>
科目: 来源: 题型:
下列有关化学反应速率的认识,正确的是
A.增大压强(对于气体反应),活化分子总数必然增大,故反应速率增大
B.温度升高,分子动能增加,减小了活化能,故反应速率增大
C.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大
D.H+和OH-的反应活化能接近于零,反应几乎在瞬间完成
查看答案和解析>>
科目: 来源: 题型:
(2008年上海卷)1.(A类题)四种短周期元素的性质或结构信息如下表,请根据信息回答下列问题:
元素 | A | B | C | D |
性质或结构信息 | 室温下单质呈粉末状固体,加热易熔化。单质在氧气中燃烧,发出明亮的蓝紫色火焰。 | 常温高压下是气体,能溶于水。原子的M层上有1个未成对的p电子 | 单质质软,因白色固体,导电性强。单质在空气中燃烧,发出黄色火焰。 | 原子最外电子层上s电子数等于p电子数。单质为空间网状晶体,具有很高的熔沸点。 |
(1)B元素在周期表中的位置是___________,写出A原子的电子排布式__________________。
(2)写出C单质与水反应的化学方程式________________________。A与C形成的化合物溶于水后,溶液的pH__________7(填“大于”、“等于”或“小于”)。
(3)D元素最高价氧化物晶体的硬度______(填“大”、“小”),其理由是__________________________。
(4)A、B两元素非金属性较强的是(写元素符号)______。写出能证明这一结论的一个实验事实__________ _____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下列实验中,能发生化学反应且反应完成后没有沉淀生成的是
A.向装有银粉的试管中滴加足量稀氨水
B.向Na2SiO3溶液中加入足量盐酸
C.向CaCl2和CH3COOH的混合溶液中加入少量Na2CO3粉末
D.向溶有SO2的 BaCl2 溶液中加入足量NaOH溶液
查看答案和解析>>
科目: 来源: 题型:
下列涉及有机物的说法正确的是
A.乙烯、氯乙烯、苯乙烯都是不饱和烃,均可用于合成有机高分子材料
B.丙烷是一种清洁燃料,可用作燃料电池的燃料
C.苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴
D.淀粉和纤维素水解产物都是葡萄糖,因此二者互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
下列实验方法正确的是
①用水鉴别四氯化碳、苯和乙醇;②用澄清石灰水鉴别碳酸钠溶液和碳酸氢钠溶液;③用闻气味的方法鉴别化纤织物和纯毛织物;④用碘水检验淀粉水解是否完全;⑤用蒸馏法分离乙酸乙酯和饱和碳酸钠溶液
A.①④ B.③④ C.②③ D.①⑤
查看答案和解析>>
科目: 来源: 题型:
某元素的一个原子形成的离子可表示为abXn-,下列说法正确的是w.w.w.k.s.5.u.c.o.m
A.a bXn-含有的中子数为a+b B.a bXn-含有的电子数为a-n
C.X原子的质量数为a+b+n D.X原子的质量约为b/6.02×1023
查看答案和解析>>
科目: 来源: 题型:
前四周期元素A、B、C、D、E、F,原子序数依次增大,其中A和B同周期,固态的AB2能升华;C和E原子都有一个未成对电子,C+比E-少一个电子层,E原子的一个电子后3p轨道全充满;D的最高化合价和最低化合价代数和为4,其最高价氧化物中D的质量分数为40%,且核内质子数等于中子数;F为红色单质,广泛用于电气工业。回答下列问题:
(1)元素电负性:D____E (填>、<或=)
(2)A、C单质熔点A_____C(填>、<或=)
(3)AE4中A原子杂化轨道方式为:________杂化;其固态晶体类型为_______
 (4)F的核外电子排布式为______;向F的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中F与NH3之间的化学键为_______
(4)F的核外电子排布式为______;向F的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中F与NH3之间的化学键为_______
(5)氢化物的沸点:B比D高的原因______;
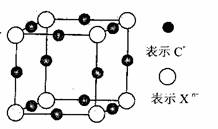
(6)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。
该晶体中阳离子和阴离子个数比为_______,晶体中每个Xn-被_____个等距离的C+离子包围。
查看答案和解析>>
科目: 来源: 题型:
解热镇痛药阿司匹林缓释片具有药效长的特点。合成路线如下:
![]()

请回答:
(1)写出反应类型:反应②_______;反应③_______________
(2)写出A的结构简式:___________
(3)写出反应①的反应方程式:_____________________________
(4)除水杨酸外,该物质的芳香族同分异构体还有_____种(要求苯环上连有两个有机基团,其中一个是羟基)。1mol阿司匹林最多消耗_______NaOH。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com