
科目: 来源: 题型:
(07年重庆卷)(14分)脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源。
(1)硫化氢与 FeCl3 溶液反应生成单质硫,其离子方程式为 _______ 。
(2)用过量NaOH溶液吸收硫化氢后,以石墨作电极电解该溶液可回收硫、其电解总反应方程式(忽略氧的氧化还原)为 ____ ;该方法的优点是______ 。
(3)一定温度下1 mol NH4 HS固体在定容真空容器中可部分分解为硫化氢和氨气。
①当反应达平衡时p氨气×p硫化氢=a(Pa2),则容器中的总压为______ Pa;
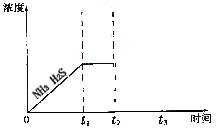
②题图是上述反应过程中生成物浓度随时间变化的示意图。若t2时增大氨气的浓度且在t3时反应再次达到平衡,请在图上画出t2时刻后氨气、硫化氢的浓度随时间的变化曲线。
查看答案和解析>>
科目: 来源: 题型:
(07年重庆卷)(14分)脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源。
(1)硫化氢与FeCl3溶液反应生成单质硫,其离子方程式为 ________ 。
(2)用过量NaOH溶液吸收硫化氢后,以石墨作电极电解该溶液可回收硫、其电解总反应方程式(忽略氧的氧化还原)为 _____ ;该方法的优点是_________ 。
(3)一定温度下1 mol NH4 HS固体在定容真空容器中可部分分解为硫化氢和氨气。
①当反应达平衡时p氨气×p硫化氢=a(Pa2),则容器中的总压为 _____ Pa;
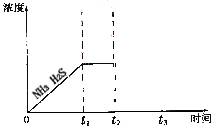
②题26图是上述反应过程中生成物浓度随时间变化的示意图。若t2时增大氨气的浓度且在t3时反应再次达到平衡,请在图上画出t2时刻后氨气、硫化氢的浓度随时间的变化曲线。
查看答案和解析>>
科目: 来源: 题型:阅读理解
我国有着丰富的海水资源,海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。镁因其合金性能卓越,在汽车、飞机制造方面很重要,有“国防金属”之称。发达国家多数从海洋中提镁,中国海水提镁技术也在不断进步。海水中虽含镁离子很多,但它是很分散的(1.28 g?L-1),要提取镁首先应让镁离子与其它离子等分离。
请回答下列问题:
(1)某化学兴趣小组利用煅烧海边贝壳所得产物,投入浓缩的海水中,最终变成了Mg(OH)2浊液。请写出最后一步反应的离子方程式: 。
(2)已知,氧化镁熔点2852℃,氯化镁的熔点714℃。无水氯化镁是工业制取镁的原料。试写出实验室蒸发氯化镁溶液制取无水氯化镁必需的实验仪器是 ;某同学对蒸发得到的固体,用酒精喷灯加热却不能熔化,请你试分析原因

(3)火力发电在江苏的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
①天然海水的pH≈8,试用离子方程式解释天然海水呈弱碱性的原因 。
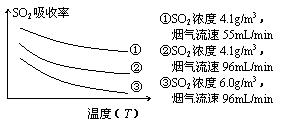 ②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如右图所示。请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议: 。
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如右图所示。请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议: 。
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,使用氧气将其氧化的化学原理是 (任写一个化学方程式或离子方程式)。氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是 。
查看答案和解析>>
科目: 来源: 题型:
(07年重庆卷)已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H―O键形成时放出热量463 kJ,则氢气中1 mol H―H键断裂时吸收热量为()
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目: 来源: 题型:
(07年重庆卷)用过量的H2SO4、NaOH、NH3?H2O、NaCl等溶液,按题12图所示步骤分开五种离子。则溶液①、②、③、④是()
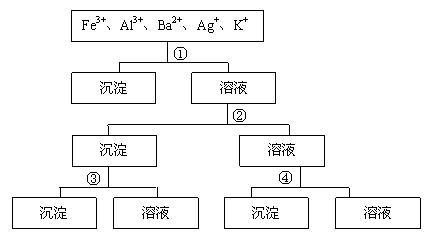
A. ①NaCl ②NaOH ③NH2?H2O ④H2SO4
B. ①H2SO4 ②NaOH ③NH3?H2O ④NaCl
C. ①H2SO4 ②NH3?H2O ③NaOH ④NaCl
D. ①NaCl ②NH3?H2O ③NaOH ④H2SO4
查看答案和解析>>
科目: 来源: 题型:
(07年重庆卷)用过量的H2SO4、NaOH、NH3?H2O、NaCl等溶液,按题12图所示步骤分开五种离子。则溶液①、②、③、④是( )

A.①NaCl ②NaOH ③NH3?H2O ④H2SO4
B.①H2SO4 ②NaOH ③NH3?H2O ④NaCl
C.①H2SO4 ②NH3?H2O ③NaOH ④NaCl
D.①NaCl ②NH3?H2O ③NaOH ④H2SO4
查看答案和解析>>
科目: 来源: 题型:
(07年重庆卷)如下图所示,下列叙述正确的是()
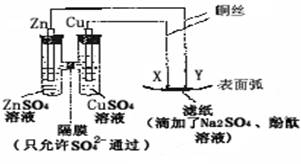
A. Y为阴极,发生还原反应
B. X为正极,发生氧化反应
C. Y与滤纸接触处有氧气生成
D. X与滤纸接触处变红
查看答案和解析>>
科目: 来源: 题型:
(07年重庆卷)用食用白醋(醋酸浓度约1 mol?L-1)进行下列实验,能证明醋酸为弱电解质的是()
A.白醋中滴入石蕊试液呈红色
B.白醋加入豆浆中有沉淀产生
C.蛋壳浸泡在白醋中有气体放出
D.pH试纸显示白醋的pH为2~3
查看答案和解析>>
科目: 来源: 题型:
(07年重庆卷)氧氟沙星是常用抗菌药,其结构简式如题9图所示,下列对氧氟沙星叙述错误的是()

A.能发生加成、取代反应 B.能发生还原、酯化反应
C.分子内共有19个氢原子 D.分子内共平面的碳原子多于6个
查看答案和解析>>
科目: 来源: 题型:
下列表格中的各种反应情况,可以用下面的曲线图象表示的是
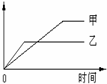
| 反应 | 纵坐标 | 甲 | 乙 |
A | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
B | 相同质量的氨,在同一容器中:2NH3 | 氨气的转化率 | 500℃ | 400℃ |
C | 在体积可变的恒压容器中,体积比1:3的N2、H2:N2+3H2 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2 mol SO2与l mol O2,相同温度下:2SO2+O2 | SO3物质的量 | 10个大 气压 | 2个大气压 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com